
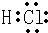 .
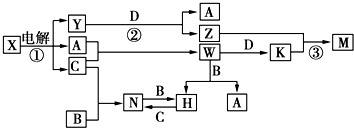
.分析 A在C中点燃有苍白色火焰,应为H2在Cl2中的燃烧,则A为H2,C为Cl2,W为HCl,应为电解饱和食盐水的反应,则X为饱和NaCl溶液,Y为NaOH,B、D是常见金属,且组成B的元素属于过渡元素,M既可溶于盐酸又可溶于NaOH溶液,能与NaOH反应生成H2的金属为Al,则D为Al,Z为NaAlO2,K为AlCl3,M为Al(OH)3,由转化关系可知B应为变价金属,应为Fe,则N为FeCl3,H为FeCl2,结合物质的性质以及题目的要求解答该题.
解答 解:A在C中点燃有苍白色火焰,应为H2在Cl2中的燃烧,则A为H2,C为Cl2,W为HCl,应为电解饱和食盐水的反应,则X为饱和NaCl溶液,Y为NaOH,B、D是常见金属,且组成B的元素属于过渡元素,M既可溶于盐酸又可溶于NaOH溶液,能与NaOH反应生成H2的金属为Al,则D为Al,Z为NaAlO2,K为AlCl3,M为Al(OH)3,由转化关系可知B应为变价金属,应为Fe,则N为FeCl3,H为FeCl2,
(1)W为HCl,W的电子式是 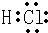 ,
,
故答案为: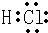 ;
;
(2)根据上面的分析可知,N为FeCl3,B为Fe,铁元素在周期表中的位置是第四周期第VIII族,
故答案为:FeCl3;第四周期第VIII族;
(3)反应①的离子方程式为2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$2Cl2↑+2H2↑+2OH-,反应③的离子方程式为3AlO2-+Al3++6H2O=4Al(OH)3↓,K为AlCl3,K溶液和过量氨水反应为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,
故答案为:2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$2Cl2↑+2H2↑+2OH-;3AlO2-+Al3++6H2O=4Al(OH)3↓;Al3++3NH3?H2O=Al(OH)3↓+3NH4+.
点评 本题考查无机物的推断,题目难度中等,根据物质的典型性质,明确物质的种类为解答该题的关键,题中注意以A在C中点燃有苍白色火焰为突破口,注意工业电解饱和食盐水的重要应用.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
| 时间(min) | n(A)(mol) | n(B)(mol) | n(C)(mol) |
| 0 | 1 | 3 | 0 |
| 第2min | 0.8 | 2.6 | 0.4 |
| 第4min | 0.4 | 1.8 | 1.2 |
| 第6min | 0.4 | 1.8 | 1.2 |
| 第8min | 0.1 | 2.0 | 1.8 |
| 第9min | 0.05 | 1.9 | 0.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6CO2(g)+6H2O(l)═C6H12O6(葡萄糖,s)+6O2(g)△H=-1880 kJ•mol-1 | |
| B. | 6CO2(g)+6H2O(l)═C6H12O6(葡萄糖,s)+6O2(g)△H=+2880 kJ•mol-1 | |
| C. | 6CO2(g)+6H2O(l)═C6H12O6(葡萄糖,s)+6O2(g)△H=+2560 kJ•mol-1 | |
| D. | 6CO2(g)+6H2O(l)═C6H12O6(葡萄糖,s)+6O2(g)△H=-1720 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 尼古丁是由26个原子构成的物质 | |
| B. | 尼古丁中C、H、N 三种元素的质量比为:10:14:2 | |
| C. | 尼古丁的相对分子质量是162g | |
| D. | 尼古丁中氮元素的质量分数为17.3% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水分子是一种极性分子,水分子空间结构呈直线型 | |
| B. | H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键 | |
| C. | 水分子间通过H-O键形成冰晶体 | |
| D. | 冰晶胞中水分子的空间排列方式与干冰胞类似 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
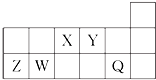
| A. | X与Y可以形成5种以上的化合物 | |
| B. | Y分别与Z、W形成的化合物的晶体类型相同 | |
| C. | 工业上常用电解法生产Z、Q的单质 | |
| D. | 简单气态氢化物的热稳定性:Y>X>W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com