
柠檬酸亚铁(FeC6H6O7)是一种易吸收的高效铁制剂,可由绿矾(FeSO4·7H2O)通过下列反应制备:
FeSO4+Na2CO3=FeCO3↓+Na2SO4
FeCO3+C6H8O7=FeC6H6O7+CO2↑+H2O
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)。
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
(1)制备FeCO3时,选用的加料方式是 (填字母),原因是 。
a.将FeSO4溶液与Na2CO3溶液同时加入到反应容器中
b.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的反应容器中
(2)生成的FeCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是 。
(3)将制得的FeCO3加入到足量柠檬酸溶液中,再加入少量铁粉,80 ℃下搅拌反应。①铁粉的作用是 。
②反应结束后,无需过滤,除去过量铁粉的方法是 。
(4)最后溶液经浓缩、加入适量无水乙醇、静置、过滤、洗涤、干燥,获得柠檬酸亚铁晶体。分离过程中加入无水乙醇的目的是 。
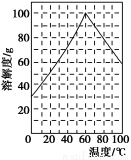
(5)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合下图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应, ,得到FeSO4溶液, ,得到FeSO4·7H2O晶体。
(1)c 避免生成Fe(OH)2沉淀
(2)取最后一次的洗涤滤液1~2 mL于试管中,向其中滴加用盐酸酸化的BaCl2溶液,若无白色沉淀产生,则表明已洗涤干净
(3)①防止+2价的铁元素被氧化 ②加入适量柠檬酸让铁粉反应完全
(4)降低柠檬酸亚铁在水中的溶解量,有利于晶体析出
(5)“(过滤,)向反应液中加入足量的铁粉,充分搅拌后,滴加NaOH溶液调节反应液的pH约为5,过滤”或“过滤,向滤液中滴加过量的NaOH溶液,过滤,充分洗涤固体,向固体中加入足量稀硫酸至固体完全溶解,再加入足量的铁粉,充分搅拌后,过滤” (滴加稀硫酸酸化,)加热浓缩得到60 ℃饱和溶液,冷却至0 ℃结晶,过滤,少量冰水洗涤,低温干燥
【解析】本题考查化学实验,意在考查考生的实验操作能力及实验设计能力,同时考查了考生对铁及其化合物性质的理解与应用能力。(1)碳酸钠溶液水解显碱性,Fe2+在碱性环境中会生成氢氧化亚铁沉淀,故应在硫酸亚铁中加入碳酸钠溶液。(2)检验FeCO3沉淀是否洗涤干净,即检验洗涤液中是否含有SO42-,可以用酸化的氯化钡溶液检验,若无白色沉淀产生,则表明已洗涤干净。(3)Fe2+具有还原性,易被空气中的氧气氧化,加入铁粉可以防止其被氧化。铁可与酸(柠檬酸)反应,故可用柠檬酸直接处理多余的铁粉,使之生成柠檬酸亚铁。(4)加入乙醇可以抑制柠檬酸亚铁在水中的溶解,提高柠檬酸亚铁的产率。(5)硫铁矿烧渣与稀硫酸反应,生成硫酸铁和硫酸铝,二氧化硅不溶于稀硫酸,故接下来的操作是“过滤”,滤液中含有铁离子和铝离子,向滤液中加入足量的强碱,铁离子以沉淀的形式析出,铝元素以偏铝酸根离子的形式存在于溶液中,再过滤,滤渣为氢氧化铁,加硫酸得到硫酸铁,然后再加铁粉生成硫酸亚铁;最后加热浓缩、冷却结晶、过滤、洗涤、低温干燥,即得硫酸亚铁晶体(绿矾)。


科目:高中化学 来源:2014年高考化学苏教版一轮复习3-2从铝土矿到铝合金练习卷(解析版) 题型:选择题
某溶液既能溶解Al(OH)3,又能溶解Al,但不能溶解Fe,在该溶液中可以大量共存的离子组是 ( )。
A.K+、Na+、HCO3-、NO3-
B.Na+、SO42-、Cl-、S2-
C.NH4+、Mg2+、SO42-、NO3-
D.H+、K+、Cl-、Na+
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习2-1物质的分类与转化 分散系练习卷(解析版) 题型:选择题
已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是( )。
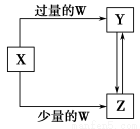
选项ABCD
XCFeCa(OH)2溶液AlCl3
WO2HNO3CO2NH3·H2O
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-2-2溶液的配制及误差分析练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列关于0.2 mol·L-1 Ba(NO3)2溶液的说法不正确的是 ( )。
A.2 L溶液中阴、阳离子总数为0.8NA
B.500 mL溶液中NO3-浓度为0.4 mol·L-1
C.500 mL溶液中Ba2+浓度为0.2 mol·L-1
D.500 mL溶液中NO3-总数为0.2NA
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-2-1物质的量 气体摩尔体积练习卷(解析版) 题型:选择题
用NA代表阿伏加德罗常数的数值,下列说法正确的是 ( )。
A.标准状况下,22.4 L CHCl3中含有的氯原子的数目为3NA
B.7 g CnH2n中含有的氢原子数目为NA
C.18 g D2O中含有的质子数目为10NA
D.0.5 mol·L-1 Na2CO3溶液中含有的CO32-的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-1-2物质的分离和提纯练习卷(解析版) 题型:选择题
下述实验不能达到预期目的的是 ( )。
编号实验内容实验目的
A将含有HCl杂质的CO2通入饱和Na2CO3溶液中除去CO2中的HCl
B将一定量的KNO3和NaCl的混合液加热并浓缩至有晶体析出,趁热过滤分离出NaCl晶体
C在含有少量FeCl3的MgCl2酸性溶液中加入足量MgO并过滤除去溶液中的FeCl3
D在含有少量Na2S的NaCl溶液中加入AgCl,再过滤除去溶液中的Na2S
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-1-1化学实验仪器及操作练习卷(解析版) 题型:填空题
某探究小组在实验室中用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝。回答下列问题:
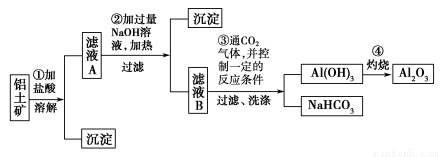
(1)在实验中需用1 mol·L-1的NaOH溶液480 mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是 。
在灼烧操作中用到下列仪器中的一种,其名称是 。
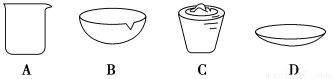
(2)写出步骤①中发生反应的离子方程式 。
(3)操作③中的洗涤操作如何进行? 。
(4)甲同学在实验室中用如图装置制备CO2气体,并通入滤液B中制备Al(OH)3时,结果没有产生预期现象。
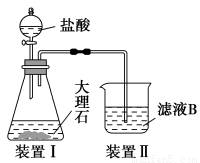
乙同学分析认为:甲同学通入CO2的量不足是导致实验失败的原因之一,你认为乙的分析是否合理? 。若合理,请用离子方程式解释其原因 (若你认为不合理,该空不作答)。
丙同学分析认为:甲同学通入的CO2中含有HCl气体,也是导致实验失败的原因,在实验中增加某装置可解决这个问题。请帮助丙同学画出该装置图,并注明试剂名称。

查看答案和解析>>
科目:高中化学 来源:2014年高考化学考前题型专练 保温训练(二)(解析版) 题型:选择题
某化学学习小组学习电化学后,设计了下面的实验装置图:
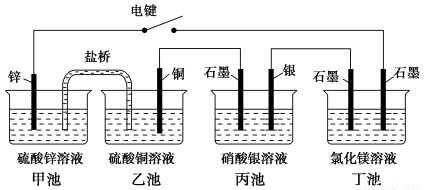
下列有关该装置图的说法中正确的是 ( )。
A.合上电键后,盐桥中的阳离子向甲池移动
B.合上电键后,丙池为电镀银的电镀池
C.合上电键后一段时间,丙池中溶液的pH增大
D.合上电键后一段时间,当丙池中生成标准状况下560 mL气体时,丁池中理论上最多产生2.9 g固体
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第8练金属及其化合物练习卷(解析版) 题型:填空题
欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。已知:碳酸不能溶解Al(OH)3沉淀。
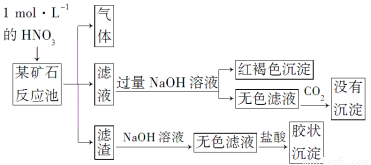
(1)Si在周期表中的位置是___________________________________。
(2)下列说法正确的是________。
a.酸性:H2CO3>H2SiO3
b.原子半径:O<C<Si<Al
c.稳定性:H2O>CH4>SiH4
d.离子半径:O2-<Al3+
(3)该矿石的组成是________,滤渣和NaOH溶液反应的离子方程式是_________________________________________________________。
(4)该矿石和1 mol·L-1HNO3反应的离子方程式为
___________________________________________________________。
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中。目的是____________________________________;
若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg,理论上至少需要1 mol·L-1 HNO3的体积为________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com