
在天平的两个托盘上,分别放上质量相等的两个烧杯,在烧杯中分别加入等质量的质量分数相等的硫酸,此时天平处于平衡状态,然后分别向两只烧杯中加入等质量的NaHCO3和Na2CO3粉末,待Na2CO3和NaHCO3完全反应,则天平两边
A.放Na2CO3的一端托盘下沉 B.放NaHCO3的端托盘下沉
C.仍保持平衡 D.无法判断
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源:2014-2015学年河南省高一12月月考理综化学试卷(解析版) 题型:选择题
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68LO2(标况下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60ml B.45ml C.30ml D.15ml
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列各组热化学方程式中,△H1> △H2 的是
①C(s)+O2(g)===CO2(g) △H1 C(s)+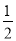 O2(g)===CO(g) △H2
O2(g)===CO(g) △H2
②S(s)+O2(g)===SO2(g) △H1 S(g)+O2(g)===SO2(g) △H2
③H2(g)+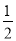 O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
④CaCO3(s)===CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)===Ca(OH)2(s) △H2
A.① B.④ C.②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:填空题
(10分)A、B、C、D、E五种物质都含钠元素,它们按图所示关系相互转化,已知A 为单质。
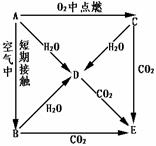
(1)该五种物质中用于焙制糕点的发酵粉及治疗胃酸过多的药品是 (填化学式)。
(2)将CO2通入E的饱和溶液中有白色沉淀生成,该反应的离子方程式为 。
(3)写出A→D、C→D、C→E反应的化学方程式
A→D:
C→D:
C→E:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:选择题
已知Na的化合价只有+1价,对于NaH+H2O===NaOH+H2↑下列说法正确的是
A.H2都是还原产物 B.H2都是氧化产物
C.NaH中的氢元素被还原 D.氧化产物与还原产物的质量相等
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.氯化钠水溶液在电流的作用下电离出Na+和Cl-
B.硫酸钡难溶于水,但硫酸钡属于强电解质
C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
D.硫酸钠在水中的电离方程式可表示为Na2SO4===2Na++S6++4O2-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一12月月考化学试卷(解析版) 题型:选择题
氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是
A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟
B.通常状况下,液氯不能用钢瓶贮存
C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照H2和Cl2的混合气体时,因迅速化合而爆炸
D.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二12月月考化学试卷(解析版) 题型:选择题
25℃时,5 mL O.1 mol /l的 H2S04和15 ml O.1 mol/lNa0H溶液相混合并稀释至500 ml,所得溶液的pH为
A.12.3 B.11 C.3 D.1.7
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省四地六校高二上学期第三次月考化学试卷(解析版) 题型:选择题
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq) ===2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O Al2O3+3H2,电解过程中,以下判断正确的是
Al2O3+3H2,电解过程中,以下判断正确的是
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3 molPb | 生成2 molAl2O3 |
C | 正极:PbO2+4H++2e-===Pb2++2H2O | 阳极:2Al+3H2O-6e-===Al2O3+6H+ |
D |
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com