
| A. | ①③ | B. | ② | C. | ③④ | D. | ①④ |
科目:高中化学 来源: 题型:选择题
| A. | 23 | B. | 55 | C. | 78 | D. | 133 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素代号 | 相关信息 |
| T | T 的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X | X 的原子最外层电子数是其内层电子数的三倍 |
| Y | 在第三周期金属元素中,Y 的简单离子半径最小 |
| Z | T、X、Z 组成的 36 电子的化合物 A 是家用消毒剂的主要成分 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同主族金属的原子半径越大熔点越高 | |
| B. | 稀有气体原子序数越大沸点越高 | |
| C. | 同周期元素的原子半径越小越易失去电子 | |
| D. | 在晶体中只要有阳离子就一定有阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
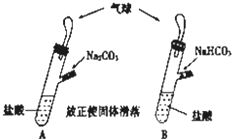 有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06g Na2CO3和0.84gNaHCO3,A、B中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06g Na2CO3和0.84gNaHCO3,A、B中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )| A. | A装置的气球膨胀速度比B快 | |
| B. | 若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L | |
| C. | 若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol/L | |
| D. | 最终两试管中Na+、Cl-的物质的量一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
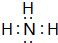 ,A和D按原子数1:1形成的化合物的结构式为H-O-O-H.
,A和D按原子数1:1形成的化合物的结构式为H-O-O-H.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com