
(8分)铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l、+2。已知Cu2O与稀硫酸反应,溶液呈蓝色,同时溶液中还存在红色浑浊。现向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol/L HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。
请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,消耗H2SO4的物质的量为 。
(4)若混合物中Cu的物质的量为n mol,则n的取值范围为 。
(8分,每空2分)(1)3 Cu2O +14 H+ + 2 NO3-= 6 Cu2+ + 2 NO↑ + 7 H2O
(2)16 g (3)0.1 mol (4)0.05<n<0.15
【解析】
试题分析:(1)Cu2O被稀HNO3氧化为Cu2+,NO3-被还原为NO,同时生成H2O,其反应的离子方程式为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O,故答案为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O;
(2)Cu、Cu2O、CuO与HNO3恰好完全反应时生成Cu(NO3)2、NO和H2O,硝酸的物质的量1L×0.6mol/L=0.6mol,NO的物质的量=2.24L÷22.4L/mol=0.1mol,根据N原子守恒可知:n[Cu(NO3)2]=(0.6mol-0.1mol)÷2=0.25mol,混合物中所含的Cu元素共有0.25mol,根据铜元素守恒可知,用H2还原Cu、Cu2O、CuO混合物后应得到0.25mol Cu,故固体的质量为0.25mol×64g/mol=16g,故答案为:16g;
(3)由Cu元素守恒可得:2×n(Cu2O)+n(CuO)+0.1mol=0.25mol,由氧化还原反应得失电子守恒可知:0.1×2+2×n(Cu2O)=0.1mol×3,解之得:n(Cu2O)=0.05mol,n(CuO)=0.05mol,混合物中,0.1mol Cu不与稀H2SO4反应,0.05molCu2O、0.05molCuO与稀H2SO4反应,根据Cu2O、CuO中氧原子与H2SO4反应结合H+生成H2O,可得n(H2SO4)=0.05mol+0.05mol=0.1mol,故答案为:0.1mol;
(4))由Cu元素守恒可得:2×n(Cu2O)+n(CuO)+n=0.25mol,由氧化还原反应得失电子守恒可知:n×2+2×n(Cu2O)=0.1mol×3,解之得:n(CuO)=n-0.05mol,n(Cu2O)=0.15mol-n,所以0.05mol<n<0.15mol,故答案为:0.05mol<n<0.15mol。
考点:考查铜及其氧化物与酸反应的有关计算


科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
根据砷元素的原子结构示意图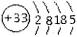 ,做出如下推理,其中与事实不符的是( )
,做出如下推理,其中与事实不符的是( )
A.砷元素位于元素周期的第四周期、第VA族
B.砷原子不如溴原子的得电子能力强
C.砷酸酸性比磷酸酸性强
D.在相同条件砷元素的氢化物的稳定性弱于氨气
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列离子方程式中,正确的是
A.次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO
B.用碳酸钠溶液吸收少量的二氧化硫: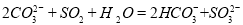
C.用食醋除去水垢中的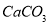 :
: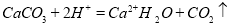
D.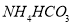 溶液与过量的
溶液与过量的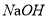 溶液反应:
溶液反应: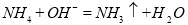
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市诸城高三10月月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.钠与CuSO4溶液反应:2Na+Cu2+==2Na++Cu
B.钠加入水中:Na+2H2O==Na++2OH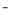 +H2↑
+H2↑
C.碳酸氢钠溶液中加入足量氢氧化钠溶液:HCO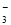 +OH
+OH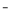 ==CO
==CO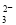 +H2O
+H2O
D.漂白粉在空气中失效:ClO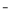 十H2O+CO2==HCO
十H2O+CO2==HCO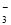 +HClO
+HClO
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市诸城高三10月月考化学试卷(解析版) 题型:选择题
下列有关实验的做法错误的是
A.用苯从溴水中提取溴,有机层从分液漏斗的上口倒出
B.实验室可以用浓氨水和生石灰制备NH3
C.实验室中用加热方法分离碘和食盐的混合物
D.加入适量的NaOH可除去NaHCO3溶液中混有的少量Na2CO3
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三10月阶段性考试化学试卷(解析版) 题型:填空题
下列关于各实验装置的叙述中不正确的是( )
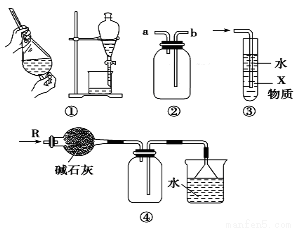
A.装置①可用于分离C2H5OH和H2O的混合物
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三10月阶段性考试化学试卷(解析版) 题型:选择题
在反应3Cl2 + 8NH3 → 6NH4Cl + N2中,设阿伏加德罗常数为NA。则下列说法正确的是( )
A.若有0.3 mol Cl2参加反应,转移的电子数为0.6NA
B.若生成2.24 L氮气,转移的电子数为0.6NA
C.若有1.2NA个电子发生转移,则被氧化的氨气的质量是27.2 g
D.若生成1 mol的氯化铵转移电子数是n个,则NA=1/n
查看答案和解析>>
科目:高中化学 来源:2015届山东省济宁市高三10月阶段测试化学试卷(解析版) 题型:填空题
(6分)实验室用固体烧碱配制500mL 0.32mol·L-1的NaOH溶液。
①需称量______ ____ g的烧碱固体,固体应放在____________中置于天平左盘称量。
②配制过程中,不需要使用的仪器是(填符号)_____________。
A烧杯 B、量筒 C、玻璃棒 D、1000mL容量瓶 E、漏斗
③根据实验的实际需要和②中列出的仪器判断,完成实验还缺少的仪器是_________ (填仪器名称)。
④由于操作上的不规范,下列使所配溶液的物质的量浓度偏低的是_________: 偏高的是______:
A称量时药品和砝码位置颠倒
B称量时间过长
C、溶液未冷却即转入容量瓶
D、容量瓶洗净后未烘干
E、定容时俯视刻度线
F、定容后倒转摇匀,发现液面低于刻度线而未加水补充
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com