
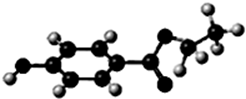
烃A与氢气以物质的量1:1发生加成反应时可以得到多种产物,以下是其中两种产物的结构简式:
|
产物 |
① |
② |
|
结构简式 |
|
|
(1)除了上述加成产物外,请写出其他加成产物的结构简式:___________(不考虑立体异构)。
(2)鉴别A与其属于芳香烃的同分异构体的试剂是________________(写化学式)。
(3)已知环外双键活泼性高于环内双键,写出产物 ② 发生聚合反应所得产物的结构简式。
_________________。
(4)双烯合成反应过程如下所示: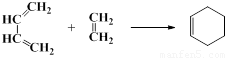
写出产物 ② 与乙烯发生双烯合成反应产物的结构简式:______________。
(5)以产物 ① 为原料通过三步反应可以转化为2-氯-3-乙基-1,4-环己二醇。
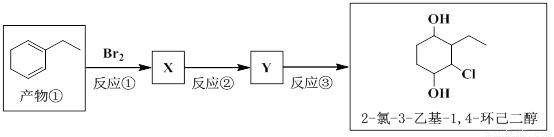
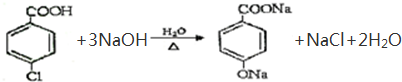
写出反应 ② 的化学方程式。_____________________。
(1)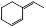 、
、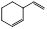 (2分);
(2分);
(2)Br2(2分);
(3)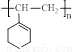 (2分);
(2分);
(4)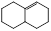 (2分);
(2分);
(5)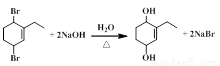 (2分)
(2分)
【解析】
试题分析:(1)发生的反应类似于1,2-丁二烯与溴的加成反应,故加成产物的结构简式: 、
、 。(2)鉴别A与其属于芳香烃应该为苯环链上连接的是烷烃基,可以通过Br2的水溶液进行鉴别,或褪色则为烯烃,若发生萃取则为芳香烃。(3)根据加成反应机理,双键中一个碳碳键打开变成单键形成链节,即可得
。(2)鉴别A与其属于芳香烃应该为苯环链上连接的是烷烃基,可以通过Br2的水溶液进行鉴别,或褪色则为烯烃,若发生萃取则为芳香烃。(3)根据加成反应机理,双键中一个碳碳键打开变成单键形成链节,即可得 。50.根据信息要形成环,首先要提供单电子,双键中必有一个键打开形成两个单键或单电子,然后再相互成键链接,故
。50.根据信息要形成环,首先要提供单电子,双键中必有一个键打开形成两个单键或单电子,然后再相互成键链接,故
产物 ②
与乙烯发生双烯合成反应产物的结构简式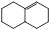 。51.①为与溴的1,4-加成反应,②卤代烃的水解反应,③为与氯化氢的马氏加成反应。反应 ②
的化学方程式
。51.①为与溴的1,4-加成反应,②卤代烃的水解反应,③为与氯化氢的马氏加成反应。反应 ②
的化学方程式 。
。
考点:本题考查结构推断,有机物的鉴别有反应类型的判断。


科目:高中化学 来源: 题型:
 .
.







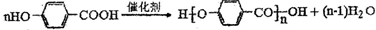
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


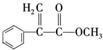
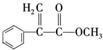



 、
、
 、
、
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
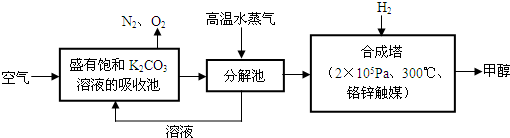
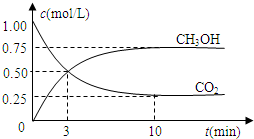
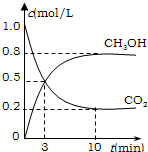 为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.
为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.| 1 |
| 2 |
| 溶解度(S)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com