
向一定量铜片中加入115mL某浓度的硫酸,在加热条件下反应,待铜片全部溶解后,将溶液稀释到500mL,再加入足量锌粉,充分反应后,收集到2.24L(标准状况)气体,过滤残留固体,干燥后称量,质量比加入的锌粉减轻了7.5g。试求:
(1)加入铜片的质量
(2)原硫酸的物质的量浓度。
(1)mcu=64g (3分) (2)CH2SO4=18.3mol.L-1 (4分)
解析试题分析:(1)生成的2.24L气体是氢气,物质的量是2.24L÷22.4L/mol=0.1mol
则根据反应式Zn+H2SO4=ZnSO4+H2↑可知,消耗锌的质量是6.5g
由于过滤残留固体,干燥后称量,质量比加入的锌粉减轻了7.5g
所以在反应Zn+CuSO4=ZnSO4+Cu中质量减少了7.5g-6.5g=1.0g
Zn+CuSO4=ZnSO4+Cu △m↓
65g 64g 1g
65g 64g 1g
即加入铜片的质量是64g
(2)根据方程式Cu+2H2SO4(浓)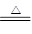 CuSO4+2H2O+SO2↑可知
CuSO4+2H2O+SO2↑可知
参加反应的浓硫酸是2mol
又因为与锌反应的稀硫酸是0.1mol
所以原浓硫酸的物质的量是2.1mol
其浓度是2.1mol÷0.115L=18.3mol/lL
考点:考查铜和浓硫酸反应的有关计算以及物质的量浓度的计算
点评:该题是高考中的常见题型和重要的考点,属于基础性试题的考查。试题基础性强,侧重对学生能力的培养和解题方法的指导和训练。该题的关键是明确反应的原理,然后再结合守恒法直接列式计算即可,有利于培养学生的逻辑推理能力,提高学生的应试能力和规范答题能力。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(6分)向一定量铜片中加入115mL某浓度的硫酸,在加热条件下反应,待铜片全部溶解后,将溶液稀释到500mL,再加入足量锌粉,充分反应后,收集到2.24L(标准状况)气体,过滤残留固体,干燥后称量,质量比加入的锌粉减轻了7.5g。
试求:
(1)加入铜片的质量。
(2)原硫酸的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年陕西省南郑中学高一下学期期中考试化学试卷(带解析) 题型:计算题
向一定量铜片中加入115mL某浓度的硫酸,在加热条件下反应,待铜片全部溶解后,将溶液稀释到500mL,再加入足量锌粉,充分反应后,收集到2.24L(标准状况)气体,过滤残留固体,干燥后称量,质量比加入的锌粉减轻了7.5g。试求:
(1)加入铜片的质量
(2)原硫酸的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源:2014届浙江省高一下学期摸底考试化学试卷 题型:计算题
向一定量铜片中加入115mL某浓度的硫酸,在加热条件下反应,待铜片全部溶解后,将溶液稀释到500mL,再加入足量锌粉,充分反应后,收集到2.24L(标准状况)气体,过滤残留固体,干燥后称量,质量比加入的锌粉减轻了7.5g。
试求:
(1)加入铜片的质量。 (2)原硫酸的物质的量浓度(结果保留一位小数)。
查看答案和解析>>
科目:高中化学 来源:2010年湖南省高三上学期第二次月考化学试题 题型:选择题
(6分)向一定量铜片中加入115mL某浓度的硫酸,在加热条件下反应,待铜片全部溶解后,将溶液稀释到500mL,再加入足量锌粉,充分反应后,收集到2.24L(标准状况)气体,过滤残留固体,干燥后称量,质量比加入的锌粉减轻了7.5g。
试求:
(1)加入铜片的质量。
(2)原硫酸的物质的量浓度。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com