
【题目】已知 25℃时,向 0.1mo/L 的碳酸氢钠溶液滴几滴酚酞,呈微红色,则该溶液中
A.若滴加甲基橙溶液呈红色
B.c(HCO3-)>c(CO32-)>c(H2CO3)
C.c(OH-)=c(H+)+ c(H2CO3)- c(CO32-)
D.若加水稀释,![]() 的比值减小
的比值减小
【答案】C
【解析】
向 0.1mo/L 的碳酸氢钠溶液滴几滴酚酞,呈微红色,则溶液pH>7,以此解题。
A.甲基橙的变色范围为3.1-4.4,当pH大于4.4时,甲基橙为黄色,故A错误;
B.0.1mol/L的碳酸氢钠溶液的pH>7,说明碳酸氢根离子的水解程度大于电离程度,但电离程度和水解程度都较小,则c(HCO3-)>c(H2CO3)>c(CO32-),故B错误;
C.溶液中存在物料守恒和电荷守恒,根据电荷守恒得c(OH-)+2c(CO32-)+c(HCO3-)=c(H+)+c(Na+),根据物料守恒得c(Na+)=c(H2CO3)+c(CO32-)+c(HCO3-),物料守恒式减去电荷守恒式得c(OH-)=c(H+)+c(H2CO3)-c(CO32-),故C正确;
D.加水稀释,促进碳酸氢根离子水解生成碳酸,因此碳酸氢根离子浓度减小,碳酸浓度增大,所以,![]() 的比值增大,故D错误;
的比值增大,故D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是

A. 离子半径的大小顺序:d<e<f
B. 与x形成简单化合物的沸点:y>z>d
C. 除去实验后试管中残留的g单质,可用热的氢氧化钠溶液
D. g、h的氧化物对应的水化物的酸性:h>g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示。则该元素对应的原子有___种不同运动状态的电子。
(2)如图2所示.每条折线表示周期表IVA–VIIA中的某一族元素氢化物的沸点变化。请解释AsH3比NH3沸点低的原因___。
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该CO2晶体属于___晶体。

(4)第一电离能介于Al、P之间的第三周期元素有__种。BCl3中B原子的杂化方式为___。
(5)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的A-D图示中正确的是__(填字母标号)。

铁原子的配位数是___,假设铁原子的半径是rcm,该晶体的密度是ρg/cm3,则铁的相对原子质量为___(设阿伏加德罗常数的值为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置进行有关Cl2的实验。下列说法不正确的是( )
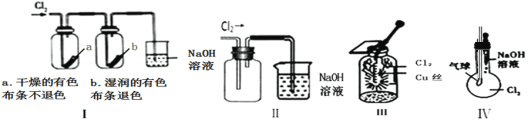
A.图I中:实验现象证明氯气无漂白作用,氯水有漂白作用
B.图II中:收集氯气
C.图IV中:若气球干瘪,证明可与NaOH溶液反应
D.图III中:生成棕黄色的烟,加少量水溶解得到蓝绿色溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁晶体([CH3CH(OH)COO]2Fe·3H2O ,相对分子质量为288)易溶于水,是一种很好的补铁剂,可由乳酸[CH3CH(OH)COOH]与FeCO3反应制得。
I.碳酸亚铁的制备(装置如图所示)
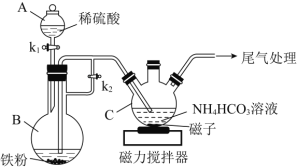
(1)实验操作如下:打开______,加入适量稀硫酸后关闭k1,使反应进行一段时间,其目的除生成FeSO4溶液外,还有__________________________________。
(2)接下来使仪器C中的制备反应发生,其反应的离子方程式为_____________。
(3)仪器C中混合物经过滤、洗涤得到FeCO3沉淀,检验其是否洗净的方法是_____。
Ⅱ.乳酸亚铁的制备及铁元素含量测定
(4)向纯净FeCO3固体中加入足量乳酸溶液,在75℃下搅拌使之充分反应,经过滤,在__________________的条件下,经低温蒸发等操作后,获得乳酸亚铁晶体。
(5)两位同学分别用不同的方案进行铁元素含量测定:
①甲同学通过KMnO4滴定法测定样品中Fe2+的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于100%,其原因可能是____________________________。
②乙同学经查阅资料后改用碘量法测定铁元素的含量计算样品纯度。称取3.000g样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成100mL溶液。吸取 25.00mL该溶液加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000 mol·L-1硫代硫酸钠溶液滴定(已知:I2 + 2S2O![]() =S4O
=S4O![]() + 2I-),当溶液_____________,即为滴定终点;平行滴定3次,硫代硫酸钠溶液的平均用量为24.80 mL,则样品纯度为_____________%。
+ 2I-),当溶液_____________,即为滴定终点;平行滴定3次,硫代硫酸钠溶液的平均用量为24.80 mL,则样品纯度为_____________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学欲探究NH3的催化氧化反应,按下图装置进行实验。A、B装置可选用的药品:浓氨水、H2O2溶液、蒸馏水、NaOH固体、MnO2。
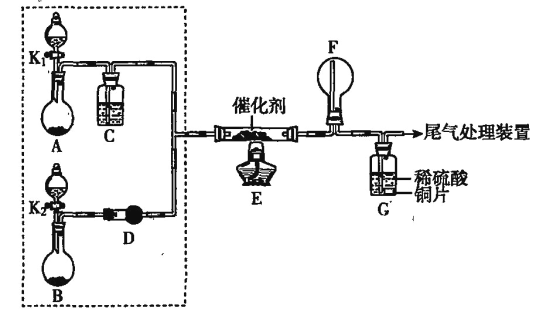
(1)NH3催化氧化的化学方程式是__________。
(2)甲、乙两同学分别按上图装置进行实验。一段时间后,装置G中的溶液都变成蓝色。
①甲观察到装置F中有红棕色气体,生成红棕色气体的化学方程式是__________。
②乙观察到装置F中只有白烟生成,白烟的成分是__________(填化学式)。
③用离子方程式解释装置G中溶液变成蓝色的原因:__________。
(3)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进:
①甲认为可调节K1和K2控制A、B装置中的产气量,应__________(填“增加”或“减少”)装置A中的产气量,或__________(填“增加”或“减少”)装置B中的产气量。
②乙认为可在装置E、F间增加置,该装置可以是__________(填字母序号)。
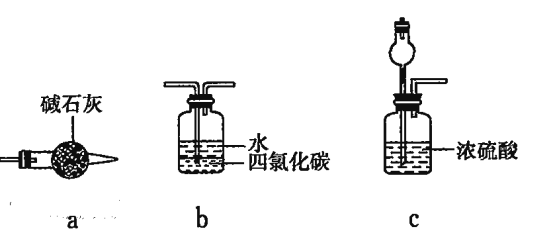
(4)为实现该反应,也可用下图所示的装置替换题.给装置中虚线框部分,
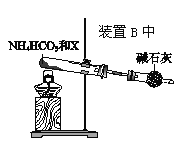
化合物X为__________。NH4HCO3的作用是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,用0.1mol/L盐酸滴定20mL0.1mol/L氨水的图像如图所示,下列说法正确的是( )

A.a点时c(Cl-)=2c(NH3H2O)+2c(NH![]() )
)
B.b点表示酸碱恰好完全反应
C.c点时c(NH![]() )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
D.a、b、c、d均有c(NH![]() )+c(H+)=c(Cl-)+c(OH-)
)+c(H+)=c(Cl-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列8种物质:①液氯;②铜;③熔融NaHSO4;④Fe(OH)3固体; ⑤ 盐酸;⑥蔗糖;⑦干冰;⑧红磷固体;⑨ AgCl; ⑩CH3COOH晶体,请按要求回答下列问题(填写物质编号)。
(1) 上述状态下能导电的是_________________________;
(2) 属于电解质是______________;
(3) 属于非电解质的是_______________;
(4) 3.1 g红磷在氯气中充分反应后,生成三氯化磷与五氯化磷的物质的量之比为1:3 , 该反应的化学方程式为___________________;
(5) 写出④与⑤反应的离子方程式________________________;
(6) 写出往NaHSO4溶液中沛加Ba(OH)2溶液至溶液呈中性时的离子方程式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com