
 离子交换膜是一类具有离子交换功能的高分子材料,在生产和科研中有广泛应用.一容器被离子交换膜分成左右两部分,如图所示:
离子交换膜是一类具有离子交换功能的高分子材料,在生产和科研中有广泛应用.一容器被离子交换膜分成左右两部分,如图所示:

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
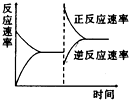 如图是关于反应A2(g)+3B2(g)?2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )
如图是关于反应A2(g)+3B2(g)?2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是( )| A、升高温度,同时加压 |
| B、降低温度,同时减压 |
| C、增大反应物浓度,同时减小生成物浓度 |
| D、增大反应物浓度,同时使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此时水的离子积KW=1×10-12 |
| B、水电离出的c(H+)=1×10-12mol.L-1), |
| C、水的电离程度随温度升高而增大 |
| D、c(Na+)=c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、中子数为20的氯原子
| ||
| B、CaH2的电子式:[H:]-Ca2+[:H]- | ||
C、铝离子结构示意图 | ||
D、比例模型 表示甲烷分子或四氯化碳分子 表示甲烷分子或四氯化碳分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、71gCl2变为Cl-可失去2NA个电子 |
| B、标准状况下1molN2和SO2的混合物的体积约占22.4L |
| C、NA个O2和NA个H2的质量比为16:1 |
| D、常温常压下4g氦气含NA个氦原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、P既是氧化剂又是还原剂,CuSO4只是还原剂 |
| B、Cu3P既是氧化产物又是还原产物 |
| C、1mol CuSO4可以氧化1/5molP |
| D、若有11molP参加反应,转移电子的物质的量为60mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3胶体有较强的吸附作用,是因为胶粒有较大的表面积 |
| B、白磷熔化、干冰汽化、SiO2熔化、AlCl3升华都是克服分子间作用力 |
| C、液晶是一种介于晶体和液体之间的中间态物质,分子较小,在信息技术中作用较大 |
| D、电解质熔融时一定能导电,因为破坏了化学键产生自由移动的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作步骤 | ①加入1ml | ②滴两滴肝脏研磨液,并混合均匀 | ③加入2ml3%的H2O2,混合均匀 | 实验结果 |
| 1号试管 | 水 | |||
| 2号试管 | 5%NaOH溶液 | |||
| 3号试管 | 5%HCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com