
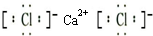 .
. 分析 (1)10Be和9Be的质子数相同、中子数不同,属于同位素;
(2)金属的金属性强弱的比较方法有:金属之间的置换反应、金属与同种酸或水生成氢气的难易程度、金属的最高价氧化物的水化物碱性强弱等来判断;
(3)和Ar核外电子排布相同的阴离子有S2-、Cl-,电子层结构相同的离子,其离子半径随着原子序数的增大而减小;其中一种离子与钾相邻元素的离子所形成的化合物可用做干燥剂,该干燥剂是CaCl2,CaCl2中阴阳离子之间存在离子键.
解答 解:(1)a.Be 元素的近似相对原子质量不等于同位素的质量数的和的一半,与与各同位素的丰度有关,故错误;
b.10Be和9Be属于同种元素的原子,化学性质相同,故正确;
c.10Be和9Be的中子数分别为6、5,所以其中子数不同,故错误;
d.化学变化中原子保持不变,则通过化学变化不能实现10Be和9Be间的相互转化,故错误;
故答案为:b;
(2)a.金属性强弱与其单质的硬度和熔点无关,故错误;
b.将空气中放置已久的这两种元素的单质分别和热水作用,二者表面都生成氧化物薄膜,氧化镁和氧化铝都不与水反应,所以无法判断金属性强弱,故错误;
c.将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液,Mg和沸水的溶液呈红色、Al和沸水的溶液不变色,说明Mg能置换出氢气,则Mg的活泼性大于Al,故正确;
d.在氯化铝和氯化镁的溶液中分别滴加过量的氢氧化钠溶液,氢氧化铝能溶于NaOH溶液,而氢氧化镁不溶于NaOH溶液,所以Mg的金属性大于Al,故正确;
故答案为:cd;
(3)和Ar核外电子排布相同的阴离子有S2-、Cl-,电子层结构相同的离子,其离子半径随着原子序数的增大而减小,所以这两种离子半径大小顺序是S2->Cl-;其中一种离子与钾相邻元素的离子所形成的化合物可用做干燥剂,该离子是钙离子,该干燥剂是CaCl2,CaCl2中阴阳离子之间存在离子键,其电子式为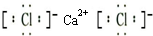 ,
,
故答案为:S2->Cl-;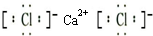 .
.
点评 本题考查较综合,涉及同位素、离子半径大小比较、金属性强弱判断、电子式等知识点,这些知识点都是考试高频点,根据基本概念及元素周期律等知识点来分析解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 由A、C两种元素的原子可形成10电子的分子 | |
| B. | F与D形成的稳定化合物能用来制作信息材料,不与任何酸反应 | |
| C. | 原子半径的大小顺序:r(E)>r(F)>r(D)>r(C) | |
| D. | 某些元素气态氢化物稳定性由强到弱的顺序:D>C>F>B |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 | B. | 滴入数滴硫酸铜溶液 | ||
| C. | 加入少量NaCl溶液 | D. | 加入少量KNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在离子化合物里,只存在离子键,没有共价键 | |
| B. | 非金属元素的两个原子之间一定形成共价键,但多个原子间也可能形成离子键 | |
| C. | 在共价化合物分子内,一定不存在离子键 | |
| D. | 由多种元素组成的多原子分子里,也可能存在非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com