
(6分) 5.3g Na2CO3 正好与20mL盐酸完全反应(Na2CO3+2HCl=2NaCl+CO2↑+H2O)。问这种盐酸的物质的量浓度c(HCl)=________________________产生的CO2在标准状况下的体积V(CO2)=_____________________
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:阅读理解
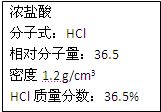 右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称量5.3g Na2CO3固体溶于480mL水配制成溶液 | B、称量5.3g Na2CO3固体溶于水配制成0.5L溶液 | C、称量5.3g Na2CO3?10H2O晶体溶于水配制成0.5L溶液 | D、称量5.3g Na2CO3?10H2O晶体溶于0.5L水配制成溶液 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖北省武汉市五校高一上学期期中统考化学试卷(带解析) 题型:计算题
(6分) 5.3g Na2CO3正好与20mL盐酸完全反应(Na2CO3+2HCl=2NaCl+CO2↑+H2O)。问这种盐酸的物质的量浓度c(HCl)=________________________产生的CO2在标准状况下的体积V(CO2)="_____________________"
查看答案和解析>>
科目:高中化学 来源:2010年湖南省长沙市高三上学期第四次月考化学卷 题型:选择题
下列叙述中正确的是(NA为阿伏加德罗常数)( )
A.通常状况下将0.5mol HI气体和0.5 mol Cl2混合后,气体的分子数小于NA
B.同温同压下,相同体积的物质,其物质的量必相等
C.5.3g Na2CO3固体含有的离子数为1.5NA
D.标准状况下,0.5 NA个Br2所占的体积约为11.2L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com