
用下图装置来做以下实验:
(1)先在玻璃容器里盛![]() 体积的氢氧化钡溶液,然后由滴定管向容器里滴入与氢氧化钡物质的量浓度相等的硫酸溶液。随着硫酸的滴入,电灯的亮度有何变化?为什么?___________
体积的氢氧化钡溶液,然后由滴定管向容器里滴入与氢氧化钡物质的量浓度相等的硫酸溶液。随着硫酸的滴入,电灯的亮度有何变化?为什么?___________
_______________________________________________________________________________。
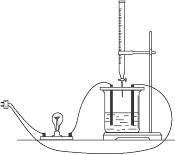
(2)根据上述实验现象能证明什么?______________________________________________。
(3)如果用氨水替代BA(OH)2,能观察到同样现象吗?为什么?_______________________
_____________________________________________________________________________。
(4)如果用盐酸替代硫酸,随着盐酸的滴入,电灯的亮度是否保持不变?为什么?______
_____________________________________________________________________________。
(1)电灯由亮逐渐变暗,直至不再发光,然后逐渐变亮;Ba(OH)2+H2SO4====BaSO4↓+2H2O,滴入H2SO4时,导电性减弱;完全反应后,H2SO4过量,导电性又增强(2)说明H2SO4与Ba(OH)2发生的反应是离子反应(3)用氨水代替Ba(OH)2不能观察到相同现象。因为H++NH3·H2O====![]() +H2O,溶液中离子浓度几乎无变化(4)用盐酸代替硫酸也不能观察到相同现象,电灯亮度基本保持不变,H++OH-====H2O,减少OH-,但增加了Cl-
+H2O,溶液中离子浓度几乎无变化(4)用盐酸代替硫酸也不能观察到相同现象,电灯亮度基本保持不变,H++OH-====H2O,减少OH-,但增加了Cl-
(1)电解质溶液导电依靠溶液中的离子,H2SO4与Ba(OH)2反应会生成难溶物BaSO4,难电离物质H2O,使离子浓度降低,直至恰好反应,离子浓度几乎为零,灯灭。2H++![]() +2OH-+Ba2+====BaSO4↓+2H2O,再加H2SO4,溶液中离子浓度变大、灯变亮。
+2OH-+Ba2+====BaSO4↓+2H2O,再加H2SO4,溶液中离子浓度变大、灯变亮。


科目:高中化学 来源:2005级高一下学期期末模拟试题(二) 题型:058
接报警,某厨房的煤气管道可能有CO泄漏,一化学兴趣小组成员受命采集该厨房的气样,并检测该气样中是否含有CO气体.
小组中一成员戴上防毒面具,进入厨房收集到一集气瓶厨房气样,他们欲用下图装置来作检测.
请回答下列问题:
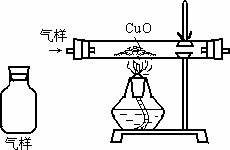
(1)采集气样时未携带抽气工具(如注射器等)如何用最简便的方法采到该瓶厨房气样?________.
(2)如何将集气瓶中的气样导入玻璃管内,请在图中画出连接示意图,并用文字作必要的说明.________.
(3)小组中有成员提出该装置产生的尾气仍有可能造成环境污染,请你提出处理尾气的方法.________.
(4)检测时通过________现象可证明厨房气样中含有CO.
(5)小组中又有成员提出,当厨房气样中CO含量很少时,用该装置做实验可能无法观察到明显现象,他们增加了一些简单的仪器和常用药品对该装置进行了改进,使得检测更为灵敏.他们是如何改进的?________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)先在玻璃容器里盛![]() 体积的氢氧化钡溶液,然后由滴定管向容器里滴入与氢氧化钡物质的量浓度相等的硫酸溶液。随着硫酸的滴入,电灯的亮度有何变化?为什么?
体积的氢氧化钡溶液,然后由滴定管向容器里滴入与氢氧化钡物质的量浓度相等的硫酸溶液。随着硫酸的滴入,电灯的亮度有何变化?为什么?
_____________________________________________________________。
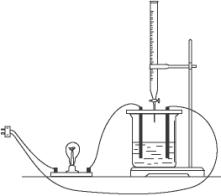
(2)根据上述实验现象能证明什么?
_________________________________________________________。
(3)如果用氨水替代Ba(OH)2,能观察到同样现象吗?为什么?
_________________________________________________________。
(4)如果用盐酸替代硫酸,随着盐酸的滴入,电灯的亮度是否保持不变?为什么?
_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省福州市毕业班质量检查理综化学试卷(解析版) 题型:选择题
(14分)过氧化钠常用做漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易变质。
(1)某课外活动小组欲探究一包过氧化钠样品是否已经变质:
取少量样品,溶解,加入_______溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。

①将仪器连接好以后,必须进行的第一步操作是_______。
②写出装置C中发生反应的化学方程式:_______。
③实验结束时,在读取实验中生成气体的体积时,你认为合理的是_______ (填选项编号)。
a.直接读取气体体积,不需冷却到室温
b.调整量筒内外液面高度使之相同
c.视线与凹液面的最低点相平读取量筒中水的体积
④读出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为_______。
⑤本实验方案存在的缺陷是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化钠常用做漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易变质。
(1)某课外活动小组欲探究一包过氧化钠样品是否已经变质:取少量样品溶解,加入_______溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该课外活动小组为了粗略测定过氧化钠的质量分数,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。
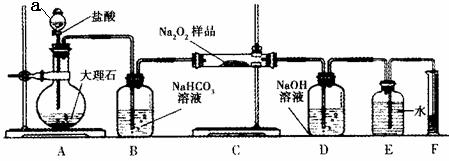
① 装置中仪器a的名称是 。
② 将仪器连接好以后,必须进行的第一步操作是_______。
③ 写出装置C中发生反应的化学方程式_______。
④ 实验结束时,在读取实验中生成气体的体积时,你认为合理的是_______ (填选项编号)。
a.直接读取气体体积,不需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com