
分析 (1)可根据Ksp[M(OH)2]=c(M2+)×c2(OH-)计算c(OH-),再根据水的离子积计算溶液中氢离子浓度;
(2)将FeCl3溶液蒸干时,铁离子水解生成Fe(OH)3和HCl,升高温度促进HCl挥发,所以蒸干溶液时得到碱,灼烧Fe(OH)3时,Fe(OH)3会分解;
(3)根据三段式解题法,求出反应混合物各组分浓度的变化量、平衡时各组分的浓度,再根据K=$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$计算平衡常数.
解答 解:(1)M(OH)2饱和溶液中c(M2+)=$\frac{1}{2}$c(OH-),则Ksp[M(OH)2]=c(M2+)×c2(OH-)=$\frac{1}{2}$c3(OH-),可知:c(OH-)=$\root{3}{2×4.0×1{0}^{-12}}$mol/L=2×10-4mol/L,则该溶液中c(H+)=$\frac{1×1{0}^{-14}}{2×1{0}^{-4}}$mol/L=5×10-11 mol/L,
故答案为:5×10-11 mol/L;
(2)将FeCl3溶液蒸干时,铁离子水解生成Fe(OH)3和HCl,升高温度促进HCl挥发,所以蒸干溶液时得到碱,灼烧氢氧化铁时,氢氧化铁会分解,反应方程式为2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,所以最终得到的是红棕色固体Fe2O3,
故答案为:Fe2O3 ;
(3)起始时c(CO)=2mol/L,平衡时CO的转化率为60%,则CO转化的浓度为:2mol/L×60%=1.2mol/L,
CO+H2O(g)?CO2 +H2,
起始(mol/L) 2 3 0 0
转化(mol/L)1.2 1.2 1.2 1.2
平衡(mol/L)0.8L 1.8 1.2 1.2
平衡时氢气浓度为1.2mol/L;
该温度下该反应的平衡常数为:K=$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$=$\frac{1.2×1.2}{0.8×1.8}$=1,
故答案为:1.2 mol/L;1.
点评 本题考查了化学平衡的计算,题目难度中等,涉及化学平衡常数计算、盐的水解原理、难溶物溶解平衡等知识,明确三段式在化学平衡计算中的应用为解答关键,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 明矾在水中形成的AI(OH)3胶体能吸收水中悬浮物,可用于水的净化 | |
| B. | Sio2是良好的半导体材料,常用于制造计算机的芯片 | |
| C. | Fe2O3俗称铁红,常用作红色的油漆和涂料 | |
| D. | 浓硫酸在常温下可用铁制容器保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,11.2LNO与11.2LO2混合后气体分子数为0.75NA | |
| B. | 7.8gNa2O2与足量的CO2反应时转移的电子数为0.2NA | |
| C. | 1L 1 mol/L的醋酸溶液中所含离子总数为2NA | |
| D. | 常温常压下,16gO3所含的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 二甲醚又称甲醚,简称DME,熔点-141.5℃,沸点-24.9℃,与石油液化气(LPG)相似,被誉为“21世纪的清洁燃料”.制备原理如下:
二甲醚又称甲醚,简称DME,熔点-141.5℃,沸点-24.9℃,与石油液化气(LPG)相似,被誉为“21世纪的清洁燃料”.制备原理如下:| 化学键 | H-H | C-O | H-O(水) | H-O(醇) | C-H |
| E/(kJ.mol-1) | 436 | 343 | 465 | 453 | 413 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
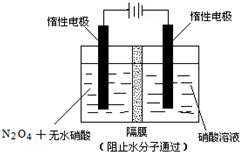 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
N2O5是一种新型硝化剂,其性质和制备受到人们的关注. .
.| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Na+、NO3-、SO42- | B. | Mg2+、NH4+、NO3-、SO42- | ||
| C. | NH4+、K+、Cl-、OH- | D. | K+、H+、SO32-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质钠放入水中,产生气体:Na+H2O═Na++OH-+H2↑ | |
| B. | 单质铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | AlCl3溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | Ca(HCO3)2溶液中加入少量NaOH:Ca2++OH-+HCO3-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只须验证它完全燃烧后产物只有H2O和CO2 | |
| B. | 只须测定其燃烧产物中H2O 和CO2 物质的量的比值 | |
| C. | 测定完全燃烧时消耗有机物与生成的H2O、CO2 的物质的量之比 | |
| D. | 测定该试样的质量及试样完全燃烧后生成H2O 和CO2 的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与该反应的压强有关 | |
| B. | 与反应的温度有关,还与反应本身有关 | |
| C. | 与化学反应本身和温度有关,并且会受到起始浓度的影响 | |
| D. | 只与化学反应本身有关,与其他任何条件无关的一个不变的常数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com