
| A. | 原子序数:b>a>c>d | B. | 最外层电子数:D>C>A>B | ||
| C. | 离子半径:C3+>D->B+>A2+ | D. | 单质的还原性:A>B>C>D |
分析 短周期元素的离子:aA2+、bB+、cC3+、dD-都具有相同的电子层结构,所以有:a-2=b-1=c-3=d+1,且A、B、C在周期表中D的下一周期,原子序数:c>a>b>d,A、B、C为金属,D为非金属.结合元素周期律递变规律解答该题.
解答 解:A.aA2+、bB+、cC3+、dD-都具有相同的电子层结构,所以有:a-2=b-1=c-3=d+1,原子序数:c>a>b>d,故A错误;
B.aA2+、bB+、cC3+、dD-都具有相同的电子层结构,其最外层电子分别为2、1、3、7,所以最外层电子数D>C>A>B,故B正确;
C.aA2+、bB+、cC3+、dD-都具有相同的电子层结构,核电荷数越大,离子半径越小,核电荷数c>a>b>d,所以离子半径D>B>A>C,故C错误;
D.同周期自左而右,金属性减弱,单质还原性减弱,则单质的还原性B>A>C,D为非金属,则单质的还原性:B>A>C>D,故D错误;
故选B.
点评 本题考查元素周期表及微粒性质比较,把握核外电子排布确定元素所在周期表中的位置及元素性质的递变规律是解答该题的关键,侧重分析与应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应中 KMnO4被氧化 | |
| B. | 氧化产物与还原产物的物质的量之比为 2:5 | |
| C. | 每生成 1 mol Cl2时,反应中转移的电子为 2 mol | |
| D. | 每消耗 16 molHCl 时,其中作氧化剂的 HCl 是 10 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) | |
| B. | 0.02mol/L的NaOH溶液与0.04mol/L的NaHC2O4溶液等体积混合液:2c(OH-)+c(C2O42-)=c(HC2O4)+2c(H+) | |
| C. | 叠氨酸(NH3)与醋酸酸性相近,0.1mol•L-1 NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-)>c(OH-)>c(H+) | |
| D. | 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
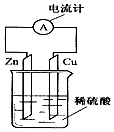
| A. | 该装置将电能转变为化学能 | B. | 电流从铜片经导线流向锌片 | ||
| C. | 一段时间后,铜片质量减轻 | D. | 锌片发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验序号 | 甲 | 乙 | 丙 |
| 混合物质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 分子中有1个手性碳原子 | B. | 遇FeCl3溶液显紫色 | ||
| C. | 1mol杀鼠灵最多能与9molH2反应 | D. | 能发生加成、取代、氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠和水反应放热 | B. | 金属钠和水反应产生可燃烧的氢气 | ||
| C. | 可在现场使用干沙灭火 | D. | 可在现场使用高压水枪灭火 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com