
常温下,将已知浓度的盐酸滴定到未知浓度的Na2CO3溶液,用pH传感器测得混合溶液的pH变化曲线,如图所示:(已知饱和CO2溶液的pH为5.6)下列说法正确的是()
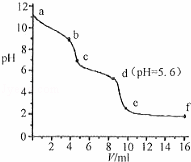
A. a点时,溶液呈碱性的原因是CO32﹣发生水解反应,其离子方程式为:CO32﹣+2H2O=H2CO3+2OH﹣
B. a→b段,溶液有气体放出
C. c点以后,盐酸过量
D. d点溶液中c(Na+)=c(Cl﹣)
考点: 中和滴定.
分析: A、碳酸根为弱酸根,水解分为两步进行,且需要可逆号;
B、a→b段,碳酸钠与盐酸反应生成碳酸氢钠,无二氧化碳气体放出;
C、c点溶液的pH=7,此时溶液呈中性,据此解答即可;
D、d点为二氧化碳的饱和溶液,此时溶液中的溶质为NaCl,据此解答即可.
解答: 解:A、碳酸根水解生成碳酸氢根,水解方程式为:CO32﹣+H2O⇌HCO3﹣+OH﹣,故A错误;
B、a→b段,碳酸钠与盐酸反应生成碳酸氢钠,离子方程式为:CO32﹣+H+⇌HCO3﹣,无气体放出,故B错误;
C、c点溶液的pH=7,此时溶液呈中性,盐酸不过量,若盐酸过量,溶液应呈酸性,故C错误;
D、d点为二氧化碳的饱和溶液,此时c(Na+)=c(Cl﹣),故D正确,故选D.
点评: 本题主要考查的是酸与盐的反应原理,涉及盐类的水解、多元弱酸根与氢离子结合的原理、pH值的应用等,综合性较强,有一定的难度.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3nm)恢复了磁性.“钴酞菁”分子的结构和性质与人体内的血红素及植物体内的叶绿素非常相似.下列说法中不正确的是( )
|
| A. | “钴酞菁”分子分散在水中所形成的分散系不具有丁达尔效应 |
|
| B. | “钴酞菁”分子能透过滤纸 |
|
| C. | 此项工作可以用来改变分子的某些物理性质 |
|
| D. | 此项工作可广泛应用于光电器件、生物技术等方面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
研究物质性质的基本程序之一就是“预测物质的性质”.下列对物质性质的预测不正确的是()
A. 乙烯双键中的一个键容易断裂,所以容易发生加成反应和取代反应
B. CH3CH3为乙烷,该物质可以看作是甲烷分子中的一个氢原子被﹣CH3取代的结果,该物质能与氯气发生取代反应
C. 某有机化合物可以表示为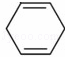 ,该物质能够使溴的四氯化碳溶液褪色
,该物质能够使溴的四氯化碳溶液褪色
D. 乙炔与苯具有相同的最简式,故等质量的苯和乙炔完全燃烧,消耗O2的质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
复盐NH4Fe(SO4)2俗称铁铵矾,下列有关其溶液的叙述正确的是()
A. 该溶液中K+、Mg2+、H+、NO3﹣不能大量共存
B. 溶液中的NH4+与Fe3+均发生水解反应,且相互促进
C. 加入金属铜与Fe3+反应的离子方程式为:2Fe3++3Cu=2Fe+3Cu2+
D. 向其中滴入Ba(OH)2溶液恰好使SO42﹣完全沉淀:NH4++Fe3++2SO42﹣+2Ba2++4OH﹣=2BaSO4↓+NH3•H2O+Fe(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做()
A. 阴极 B. 阳极 C. 正极 D. 负极
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2O4+8H2O 3Zn(OH)2+2Fe(OH)3+2Fe(OH)3+4KOH下列叙述不正确的是()
3Zn(OH)2+2Fe(OH)3+2Fe(OH)3+4KOH下列叙述不正确的是()
A. 放电时负极反应为:3Zn﹣6e﹣+6OH﹣═3Zn(OH)2
B. 放电时正极反应为:2FeO42﹣+6e﹣+8H2O═2Fe(OH)3+10OH﹣
C. 放电时每转移3mol电子,正极有1mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下体积固定的容器中,可以充分说明可逆反应A(g)+3B(g)⇌3C(g)+D(g),达到平衡状态的是()
A. 器内压强不随时间变化而变化
B. 反应器内A、B、C、D物质的量比为1:3:3:1
C. 生成A的速率和生成的D的速率相等
D. 生成 1mol A同时有3 mol C被消耗
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列物质中少量杂质的方法不正确的是()
A. 除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
B. 除去CO2中混有的HCl:用饱和NaHCO3溶液洗气
C. 除去BaCO3固体中混有的BaSO4:加入过量的盐酸、过滤、洗涤
D. 除去甲烷中混有的乙炔:通过溴水溶液后,洗气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com