
·ÖĪö øł¾Ż°¢·ü¼ÓµĀĀŽ¶ØĀÉæÉÖŖ£¬Ķ¬ĪĀĶ¬Ń¹ĻĀĶ¬Ģå»żµÄN2ŗĶCO2µÄĪļÖŹµÄĮæĻąĶ¬£¬øł¾Ż·Ö×ÓµÄ×é³ÉŗĶ·Ö×ÓµÄĻą¶Ō·Ö×ÓÖŹĮæ¼ĘĖćĮ£×ÓøöŹżŅŌ¼°ÖŹĮ攢ĆÜ¶ČµČ¹ŲĻµ£®
½ā“š ½ā£ŗøł¾Ż°¢·ü¼ÓµĀĀŽ¶ØĀÉæÉÖŖ£¬Ķ¬ĪĀĶ¬Ń¹ĻĀĶ¬Ģå»żµÄN2ŗĶCO2µÄĪļÖŹµÄĮæĻąĶ¬£¬ĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£»
ÉčN2ŗĶCO2µÄĪļÖŹµÄĮ涼ĪŖ1mol£¬
Ōņøł¾ŻN=n•NAæÉÖŖ£ŗĘųĢåµÄ·Ö×ÓŹżÖ®±ČµČÓŚĪļÖŹµÄĮæÖ®±Č£¬ĪŖ1£ŗ1£»
1øöCO2ÖŠŗ¬ÓŠ3øöŌ×Ó£¬1øöN2ÖŠŗ¬ÓŠ2øöŌ×Ó£¬ŌņŌ×ÓŹżÖ®±Č=1”Į2£ŗ£Ø1”Į3£©=2£ŗ3£»
1molN2µÄÖŹĮæĪŖ£ŗ1mol”Į28g/mol=28g£¬1molCO2µÄÖŹĮæĪŖ£ŗ1mol”Į44g/mol=44g£¬N2ŗĶCO2µÄÖŹĮæÖ®±ČĪŖ28£ŗ44=7£ŗ11£»
ŅņN2ŗĶCO2µÄĢå»żĻąĶ¬£¬ŌņĆܶČÖ®±ČµČÓŚÖŹĮæÖ®±Č=7£ŗ11£¬
¹Ź“š°øĪŖ£ŗ1£ŗ1£»1£ŗ1£»2£ŗ3£»7£ŗ11£»7£ŗ11£®
µćĘĄ ±¾Ģā漲鰢·ü¼ÓµĀĀŽ¶ØĀɼ°ĘäĶĘĀŪ£¬ĢāÄæÄŃ¶Č²»“ó£¬Ć÷Č·ĪļÖŹµÄĮæÓėĘäĖüĪļĄķĮæÖ®¼äµÄ¹ŲĻµ¼“æɽā“š£¬×¢ŅāĻą¹Ų¼ĘĖć¹«Ź½µÄŌĖÓĆ£¬ŹŌĢāÅąŃųĮĖѧɜµÄ»Æѧ¼ĘĖćÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.5mL | B£® | 0.1mL | C£® | 0.05mL | D£® | 0.01mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ±ąŗÅ | H2C2O4ČÜŅŗ | ĖįŠŌKMnO4ČÜŅŗ | ĪĀ¶Č”ę | ||
| ÅضČ/£Ømol•L-1£© | Ģå»ż/mL | ÅضČ/£Ømol•L-1£© | Ģå»ż/mL | ||
| ¢Ł | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ¢Ś | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ¢Ū | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
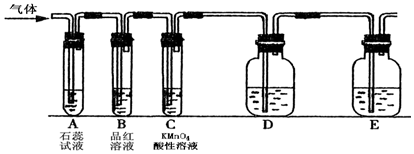
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
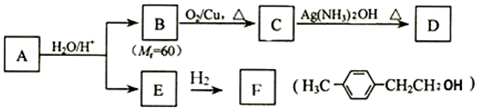
 £®
£® £ØĘäÖŠŅ»ÖÖ£©£®
£ØĘäÖŠŅ»ÖÖ£©£® £©µÄŗĻ³ÉĀ·Ļߣ®
£©µÄŗĻ³ÉĀ·Ļߣ®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ²»“æĪļÖŹ | ³żŌÓŹŌ¼Į | ·ÖĄė·½·Ø | ±ŲÓĆŅĒĘ÷ |
| A | µā£ØĖ®£© | ĖÄĀČ»ÆĢ¼ | ŻĶČ” | ·ÖŅŗĀ©¶· |
| B | ĀČ»Æ¼Ų£ØĀČ»ÆøĘ£© | ŹŹĮæŃĪĖį | ¹żĀĖ | ²£Į§°ō |
| C | ĻõĖįĶ£ØĻõĖįŅų£© | ŹŹĮæĶ·Ū | ½į¾§ | ¾Ę¾«µĘ |
| D | ĮņĖį¼Ų£ØĢ¼Ėį¼Ų£© | ŹŹĮæŃĪĖį | ÕōĮó | ĪĀ¶Č¼Ę |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ½«2.32g Na2CO3”¢NaOHµÄ¹ĢĢå»ģŗĻĪļĶźČ«ČܽāÓŚĖ®£¬ÖĘ³ÉČÜŅŗ£¬Č»ŗóĻņøĆČÜŅŗÖŠÖšµĪ¼ÓČė1mol/LµÄŃĪĖį£¬Ėł¼ÓŃĪĖįµÄĢå»żÓė²śÉśCO2µÄĢå»ż£Ø±ź×¼×“æö£©¹ŲĻµČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ£Ø””””£©
½«2.32g Na2CO3”¢NaOHµÄ¹ĢĢå»ģŗĻĪļĶźČ«ČܽāÓŚĖ®£¬ÖĘ³ÉČÜŅŗ£¬Č»ŗóĻņøĆČÜŅŗÖŠÖšµĪ¼ÓČė1mol/LµÄŃĪĖį£¬Ėł¼ÓŃĪĖįµÄĢå»żÓė²śÉśCO2µÄĢå»ż£Ø±ź×¼×“æö£©¹ŲĻµČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÖŠ“ķĪóµÄŹĒ£Ø””””£©| A£® | OA¶Ī·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗH++OH-ØTH2O CO32-+H+ØTHCO3- | |
| B£® | AµćČÜŅŗÖŠµÄČÜÖŹĪŖNaCl”¢NaHCO3 | |
| C£® | »ģŗĻĪļÖŠNaOHµÄÖŹĮæ0.60 g | |
| D£® | µ±¼ÓČė35 mLŃĪĖįŹ±£¬²śÉśCO2µÄĢå»żĪŖ224 mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
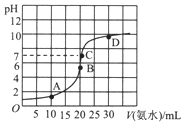 ³£ĪĀĻĀ£¬Ļņ20mlÅضČĪŖ0.1000mol/LµÄŃĪĖįÖŠÖšµĪ¼ÓČė0.1000mol/LµÄ°±Ė®£¬pHĖę°±Ė®Ģå»żµÄ±ä»ÆČēĶ¼£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
³£ĪĀĻĀ£¬Ļņ20mlÅضČĪŖ0.1000mol/LµÄŃĪĖįÖŠÖšµĪ¼ÓČė0.1000mol/LµÄ°±Ė®£¬pHĖę°±Ė®Ģå»żµÄ±ä»ÆČēĶ¼£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ŌŚBµćŹ±£ŗc£ØH+£©=c£ØOH-£©+c£ØNH3•H2O£© | |
| B£® | ŌŚCµćŹ±£ŗc£ØCl-£©£¼c£ØNH4+£©+c£ØNH3•H2O£© | |
| C£® | AµćÓėBµćĻą±Č£ŗ2n£ØNH4+£©£¾n£ØNH4+£© | |
| D£® | “ÓCµ½DµÄ¹ż³ĢÖŠ£¬æÉÄܳöĻÖ£ŗc£ØCl-£©£¾c£ØNH4+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó | ½įĀŪ |
| A | Č”µČĪļÖŹµÄĮæµÄĮ½ÖÖ½šŹōµ„ÖŹX”¢Y£¬·Ö±šÓė×ćĮæµÄŃĪĖį·“Ó¦ | X²śÉśĒāĘųµÄĢå»ż±ČY¶ą | ½šŹōŠŌ£ŗX£¾Y |
| B | ÓĆ²£Į§°ōÕŗČ”ÅØĮņĖįµćµ½Ą¶É«ŹÆČļŹŌÖ½ÉĻ | ŹŌÖ½±äŗŚ | ÅØĮņĖį¾ßÓŠĶŃĖ®ŠŌ |
| C | ½«ÕŗÓŠÅØ°±Ė®µÄ²£Į§°ōÖĆÓŚÄ³ĪŽ»śĖįÅØČÜŅŗµÄŹŌ¼ĮĘææŚ | ÓŠ“óĮæ°×ŃĢ | øĆĪŽ»śĖįŅ»¶ØĪŖŃĪĖį |
| D | Č”¾ĆÖƵÄNa2O2·ŪÄ©£¬ĻņĘäÖŠµĪ¼Ó¹żĮæµÄŃĪĖį | ²śÉśĪŽÉ«ĘųĢå | Na2O2ƻӊ±äÖŹ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com