
|
为确定某溶液的离子组成,进行如下实验: ①测定溶液的 pH,溶液显强碱性;②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体; ③向上述溶液中再滴加 Ba(NO3)2溶液,产生白色沉淀;④取上层清液继续滴加 Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,又产生了白色沉淀.根据实验现象,以下推测不正确的是 | |
| [ ] | |
A. |
一定有 SO42- |
B. |
一定有 CO32- |
C. |
不能确定 Cl-是否存在 |
D. |
不能确定 HCO3-是否存在 |
|
讲析:解答本题时,要将实验过程和备选答案结合起来进行分析.因为溶液呈强碱性,所以溶液中肯定不含有 HCO3-;实验②说明溶液中肯定含有CO32-;实验③说明溶液中肯定含有SO42-.因为实验②中引入了Cl-,所以实验④无法说明原溶液中是否含有Cl-.点拨:解离子共存问题,除了要熟悉常见离子的性质外,还要注意题设情景,即能否共存的环境及要求.如酸性、碱性环境,无色透明溶液,产生气体、沉淀,“一定能大量共存”、“可能大量共存”、“能大量共存”或“不能大量共存”等.根据离子反应推断物质成分时要注意以下几个关键点:①结合实验现象推出肯定存在或肯定不存在的物质或离子;②在肯定某些离子存在的同时,结合离子共存规律,否定一些离子的存在(简称互斥性原则);③注意实验过程中生成的离子或引入的离子对后续实验的干扰(简称进出性原则);④明确溶液中既要有阳离子,也要有阴离子(简称电中性原则). |


科目:高中化学 来源: 题型:
| (c+d) | 2 |




查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原溶液中肯定不含Fe2+、Mg2+、SiO32- | B、步骤Ⅱ中无色气体可能含有CO2,原溶液中可能含有CO32- | C、原溶液中肯定含有K+、Fe2+、NO3-、SO42-、I- | D、为确定是否含有Cl-,可取原溶液加入少量硝酸银和稀硝酸,观察是否产生沉淀 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山西省高三上学期第二次阶段性测试化学试卷 题型:填空题
(10分)A~H有如图所示的转化关系,其中A是盐,B、C、D、E、F在常温常压下均是气态物质,反应④、⑤均在溶液中进行,转化中反应条件略去。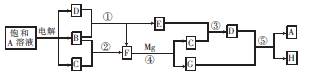
试回答下列问题:
(1)物质A的化学式为 ,电解时阴极反应式为 .
(2)反应③的化学方程式为 。
(3)反应⑤的离子方程式为 。
(4)镁与铝能形成多种合金,为了确定某合金样品的成分,小明同学设计如图所示的实验步 骤,确定合金组成。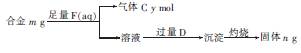
①能确定合金组成的数据组有 (填字母)。
a.m、n b.m、y c.n、y
②若合金中Mg的物质的量分数为x,金属总物质的量为7 mol,试在图中作出y随x变化的曲线。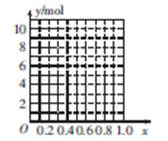
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com