
 氮可形成多种氧化物,如NO、NO2、N2O4等.
氮可形成多种氧化物,如NO、NO2、N2O4等.| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
分析 (1)0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,反应为2NO2+2NaOH═NaNO3+NaNO2+H2O,得到溶液中NaNO3物质的量浓度为0.mol/L,NaNO2物质的量为0.1mol/L,溶液B为0.1mol•L-1的CH3COONa溶液,已知HNO2的电离常数Ka=7.1×10-4mol•L-1,CH3COOH的电离常数Ka=1.7×10-5mol•L-1,说明CH3COOH酸性小于HNO2的酸性,对应阴离子水解程度大,据此分析判断;
(2)①根据v=$\frac{△c}{△t}$计算v(N2O4),再利用速率之比等于化学计量数之比计算v(NO2);
60min、80min时N2O4的物质的量相等,说明60min时,反应到达平衡;
平衡时,N2O4的浓度为$\frac{0.08mol}{2L}$=0.04mol/L,NO2的浓度是$\frac{0.4mol}{2L}$-0.04mol/L×2=0.12mol/L,再根据K=$\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$计算平衡常数;
②若在相同条件下,最初向该容器充入的是N2O4气体,达到上述同样的平衡状态,为等效平衡,则N2O4完全转化可以得到0.4molNO2,平衡时N2O4的物质的量相等;
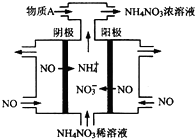
(3)电解NO制备NH4NO3,由图可知,乙为阳极反应为:5NO-15e-+10H2O=5NO3-+20H+,甲为阴极反应为:3NO+15e-+18H+=3NH4++3H2O,电池总反应方程式为:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3;
解答 解:(1)0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,反应为2NO2+2NaOH═NaNO3+NaNO2+H2O,得到溶液A中NaNO3物质的量浓度为0.mol/L,NaNO2物质的量为0.1mol/L,溶液B为0.1mol•L-1的CH3COONa溶液,已知HNO2的电离常数Ka=7.1×10-4mol•L-1,CH3COOH的电离常数Ka=1.7×10-5mol•L-1,说明CH3COOH酸性小于HNO2的酸性,对应阴离子水解程度大,醋酸根离子和亚硝酸根离子水解,两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为:c(NO3-)>c(NO2-)>c(CH3COO-);
使溶液A和溶液B的pH值相等的方法,依据溶液组成和性质分析,溶液A中NaNO3物质的量浓度为0.mol/L,NaNO2物质的量为0.1mol/L,溶液B为0.1mol•L-1的CH3COONa溶液,溶液B碱性大于A溶液;
a、上述分析可知,溶液B碱性大于A溶液,向溶液A中加适量水,稀释溶液,减小减小,不能调节溶液PH相同,故a不符合;
b、向溶液A中加适量NaOH,增大碱性,可以调节溶液pH相同,故b符合;
c、向溶液B中加适量水,稀释溶液碱性减弱,可以调节溶液pH,故c符合;
d、溶液B碱性大于A溶液,向溶液B中加适量NaOH,溶液PH更大,不能调节溶液PH相同,故d不符合;
故答案为:c(NO3-)>c(NO2-)>c(CH3COO-);bc;
(2)①20s内v(N2O4)=$\frac{\frac{0.05mol}{2L}}{\frac{1}{3}min}$=0.075mol/(L.s),速率之比等于化学计量数之比,v(NO2)=2v(N2O4)=0.15mol/(L.min);
60min、80min时N2O4的物质的量相等,说明60min时,反应到达平衡,所以n3=n4;
平衡时,N2O4的浓度为$\frac{0.08mol}{2L}$=0.04mol/L,NO2的浓度是$\frac{0.4mol}{2L}$-0.04mol/L×2=0.12mol/L,故平衡常数K=$\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$=$\frac{0.04}{0.1{2}^{2}}$=2.8,
故答案为:0.15;=;2.8;
②若在相同条件下,最初向该容器充入的是N2O4气体,达到上述同样的平衡状态,为等效平衡,则N2O4完全转化可以得到0.4molNO2,则N2O4的起始物质的量为$\frac{1}{2}$×0.4mol=0.2mol,N2O4的起始浓度为$\frac{0,2mol}{2L}$=0.1mol/L,平衡时N2O4的物质的量为0.08mol,故N2O4的转化率为$\frac{02mol-0.08mol}{0.2mol}$×100%=60%,
故答案为:0.1;60%;
(3)电解NO制备NH4NO3,由图可知,乙为阳极反应为:5NO-15e-+10H2O=5NO3-+20H+,甲为阴极反应为:3NO+15e-+18H+=3NH4++3H2O,电池总反应方程式为:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3,电解产生的硝酸多,需补充NH3,
故答案为:NH3;根据反应:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3,电解产生的硝酸多,需补充NH3;
点评 本题考查化学平衡计算与影响因素、化学平衡常数、盐类水解、离子浓度大小比较、电解原理等知识,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及灵活应用基础知识的能力,需要学生具备扎实的基础与灵活应用能力,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4g金属镁变成镁离子时失去的电子数目为0.1NA | |
| B. | 标准状况下,2.24LBr2所含的分子数为0.1NA | |
| C. | 室温下,32gO2和O3的混合气体中含有的氧原子数为2NA | |
| D. | 1.0mol•L-1的Na2CO3溶液中含有的Na+离子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定是酸的溶液 | B. | 一定是碱的溶液 | ||
| C. | 一定是碱性溶液 | D. | 可能是酸性溶液也可能是碱性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
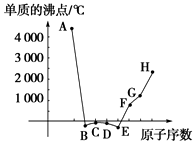 A、B、C、D、E、F、G、H为八种相邻的短周期元素,其单质的沸点如图所示.
A、B、C、D、E、F、G、H为八种相邻的短周期元素,其单质的沸点如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | n(CO)/mol | n(Cl2)/mol |
| 0 | 1.20 | 0.6 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
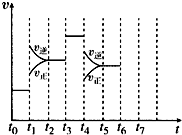 在一密闭容器中发生反应N2+3H2 2NH3△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
在一密闭容器中发生反应N2+3H2 2NH3△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com