
| A. | 硫酸和醋酸反应时放出氢气一样多 | B. | 反应后醋酸溶液中锌粉有剩余 | ||
| C. | 稀释后溶液中的c(H+)硫酸比醋酸大 | D. | 反应开始时醋酸中的反应速率大 |
分析 pH均等于1的硫酸和醋酸各10ml,分别稀释10倍后,硫酸溶液PH变化为2,醋酸溶液PH<2,pH=2的硫酸溶液中氢离子浓度为0.01mol/L,硫酸物质的量=0.01mol/L×0.1L=0.001mol,硫酸完全反应需要锌的质量0.001mol×65g/mol=0.065g<0.07g,所以Zn有剩余,醋酸是弱酸,其物质的量大于0.001mol,据此分析解答.
解答 解:A.pH均等于1的硫酸和醋酸各10ml,醋酸溶液浓度大于硫酸,分别稀释10倍后,加入0.07g锌反应,若锌都剩余或全部反应,则醋酸生成氢气多,故A错误;
B.醋酸浓度大于硫酸,醋酸溶液中可能剩余锌,也可能全部反应,故B错误;
C.醋酸存在电离平衡,稀释后醋酸溶液中氢离子浓度大于硫酸,故C错误;
D.pH均等于1的硫酸和醋酸各10ml,分别稀释10倍后,硫酸溶液PH变化为2,醋酸溶液PH<2,醋酸溶液中氢离子浓度大,加入锌反应速率快,故D正确;
故选D.
点评 本题考查弱电解质的电离,首先要根据酸和金属质量进行过量计算,注意:反应速率与氢离子浓度成正比,与酸的强弱无关,为易错点,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 4:11 | B. | 16:9 | C. | 8:11 | D. | 32:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R一定是非金属元素 | B. | R的最高价氧化物为R2O5 | ||
| C. | 最高价氧化物对应水化物H2RO4 | D. | R的气态氢化物为RH5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
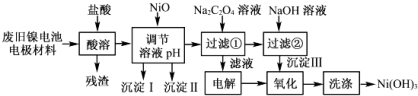
| M(OH)n | Ksp | 开始沉淀pH | 沉淀完全pH |
| Al(OH)3 | 1.9×10-23 | 3.4 | 4.2 |
| Fe(OH)3 | 3.8×10-38 | 2.5 | 2.9 |
| Ni(OH)2 | 1.6×10-14 | 7.6 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/LNaCl溶液含有nA个Na+ | |
| B. | 0.1molOH-含nA个电子 | |
| C. | 1molCu和足量稀硝酸反应产生nA个NO分子 | |
| D. | 常温常压下,22.4LCO2中含有nA个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
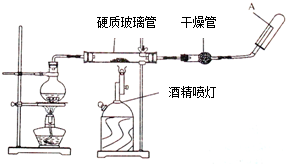 在常温下,Fe 与水并不发生反应,但在高温下,Fe 与水蒸气可以发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,即可以完成高温下Fe 与水蒸气的反应实验.
在常温下,Fe 与水并不发生反应,但在高温下,Fe 与水蒸气可以发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,即可以完成高温下Fe 与水蒸气的反应实验.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com