

���� A�����Ʊ�����������MnO2+2Cl-+4H+ $\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��B��C���ڳ��ӣ��ֱ��ȥ�Ȼ����ˮ��ʵ�鿪ʼǰ����D�з���һ��������ۣ�����ʹ���ۻ���Ȼ��ת����ҡ����ƿʹ��������ƿ�ڱڱ����γ�һ���㣬���������������ĽӴ���������ڳ�ַ�Ӧ������Ȼ�����ˮ�ֽ⣬F���ڷ�ֹ�����е�ˮ��������װ�ã�������������ֹ��Ⱦ�������Դ˽����⣮
��1���Ƶõ����������������Ȼ����ˮ��Ӧ��ȥ��
��2���ɷ�ĩ״��Ϊһ���㣬�����˷�Ӧ�Ӵ�������ܼӿ췴Ӧ���ʣ�ʹ��Ӧ��֣�
��3��ʵ��ʱ��Dװ���������50-59�����ˮԡ�¶�0-100�棬��ò���ˮԡ���ȵķ�ʽ����ȴ�ñ�ˮ��ȴ��
��4�����Ȼ�����ˮ�ֽ⣬Ҫ����������ˮ�ĸ��ţ�
��5�����Ȼ�����SO3���������������ȺͶ�������
��� �⣺��1��ʵ�����ö������̺�Ũ������ȡ������Ũ�����ӷ��������Ƶõ����������������Ȼ����ˮ����ȥ�Ȼ����ñ���ʳ��ˮ��Ũ���������ˮ�ԣ���ˮ��Ũ���ᣬ
�ʴ�Ϊ������ʳ��ˮ��Ũ���
��2��ʵ�鿪ʼǰ����D�з���һ��������ۣ�����ʹ���ۻ���Ȼ��ת����ҡ����ƿʹ��������ƿ�ڱڱ����γ�һ���㣬���������������ĽӴ���������ڳ�ַ�Ӧ���ܼӿ췴Ӧ���ʣ�
�ʴ�Ϊ������Ӧ�ĽӴ������
��3��ʵ��ʱ��Dװ���������50-59�����ˮԡ�¶�0-100�棬����ˮԡ���ȵķ�ʽ�����Ȼ���SCl2���۵�-78�棬���Խ���ƿ�����ˮ����ȴ����ֹE��Һ����Ȼ���SCl2���ӷ���
�ʴ�Ϊ��ˮԡ���ȣ�����ƿ�����ˮ����ȴ��
��4�����Ȼ�����ˮ�ֽ⣬Ҫ����ˮ����ʯ�ң�������������ƻ���ʯ�ң�������������ˮ�ĸ��ţ���ֹ������ˮ�������벢���ղ������������
�ʴ�Ϊ����ʯ�ң�������������ƻ���ʯ�ң�����ֹ������ˮ�������벢���ղ������������
��5������Ԫ���غ��֪�����Ȼ�����SO3���������������ȵĻ�ѧ����ʽΪSCl2+SO3=SOCl2+SO2 ��
�ʴ�Ϊ��SCl2+SO3=SOCl2+SO2��
���� ��������������ϳɶ��Ȼ����ʵ��Ϊ���壬�����Ķ���ȡ��Ϣ����������ʵ��ԭ������ȣ�Ϊ��Ƶ���㣬����ѧ���ķ�����ʵ�������Ŀ��飬�Ƕ�֪ʶ���ۺ����ã�����ʵ��ԭ���ǽ���Ĺؼ�����Ҫѧ��������ʵ�Ļ������ۺ����÷�����������������ע�������Ŷ��Ȼ�����ˮ�ֽ�Ϊ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ӧ�����ƶ� | B�� | ���淴Ӧ�����ƶ� | ||
| C�� | �ﵽƽ�� | D�� | ���ж��ƶ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
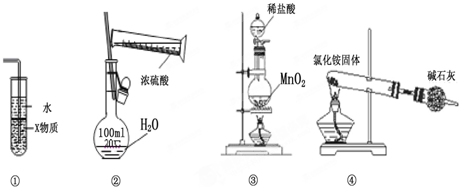
| A�� | װ���Т�X��Ϊ���Ȼ�̼�����װ�ÿ��������հ���������ֹ���� | |
| B�� | װ�âڿ�����ʵ��������һ�����ʵ���Ũ�ȵ�ϡ���� | |
| C�� | ʵ������װ�â���ȡ���� | |
| D�� | ʵ������װ�â���ȡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ˮ��CH3COOH=CH3COO-+H+ | |
| B�� | ����״̬�µ�NaHSO4��NaHSO4=Na++H++SO42- | |
| C�� | ̼����������ˮ��NaHCO3=HCO3-+Na+ | |
| D�� | ��������ˮ��H2S?2H++S2- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com