
 .
.分析 A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大.A和E最外层电子数相同,二者同主族,短周期主族元素的原子中,E原子的半径最大,则E为Na;B、C和F在周期表中相邻,B、C同周期,C、F同主族,则B、C处于第二周期,F处于第三周期,F原子的质子数是C原子质子数的2倍,则C为O元素、F为S元素,可知B为N元素;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y ),则A为H元素,X为H2O、Y为H2O2;D形成的分子为双原子分子,且原子序数介于氧、钠之间,故D为F元素;G的原子序数大于硫,故G为Cl,据此解答.
解答 解:A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大.A和E最外层电子数相同,二者同主族,短周期主族元素的原子中,E原子的半径最大,则E为Na;B、C和F在周期表中相邻,B、C同周期,C、F同主族,则B、C处于第二周期,F处于第三周期,F原子的质子数是C原子质子数的2倍,则C为O元素、F为S元素,可知B为N元素;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y ),则A为H元素,X为H2O、Y为H2O2;D形成的分子为双原子分子,且原子序数介于氧、钠之间,故D为F元素;G的原子序数大于硫,故G为Cl.
(1)由上述分析可知,D为氟元素,F形成的离子为S2-,离子结构示意图为: ,故答案为:氟;
,故答案为:氟; ;
;
(2)液态化合物Y为H2O2,一定浓度的H2O2溶液作消毒剂,故答案为:一定浓度的H2O2溶液作消毒剂;
(3)用某种金属易拉罐与A、C、E组成的化合物NaOH的水溶液反应,产生的气体可充填气球,是Al与氢氧化钠反应生成偏铝酸钠与氢气,该反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑,使用这种气球存在的隐患是:氢气易燃、易爆,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;氢气易燃、易爆;
(4)P和Q两种物质都是由H、O、Na、S四种元素组成的盐,其水溶液都显酸性,两物质为NaHSO3、NaHSO4,等物质的量的P和Q恰好完全反应,该反应的离子方程式:H++HSO3-═SO2↑+H2O,
故答案为:H++HSO3-═SO2↑+H2O;
(5)H、N、Cl三种元素两两组合形成的化合物在空气中相遇形成白烟,是氨气与HCl反应生成氯化铵,反应的化学方程式为:NH3+HCl═NH4Cl,
故答案为:NH3+HCl═NH4Cl.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素化合物性质的掌握,难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1s、2px、2py、2pz轨道都具有球对称性 | |
| B. | 因为p轨道是“8”字形的,所以p电子也是“8”字形 | |
| C. | 氢原子中只有一个电子,故氢原子只有一个轨道 | |
| D. | 原子轨道示意图与电子云图都是用来形象描述电子运动状态的图形 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某混合溶液中可能含有的离子如表所示:
某混合溶液中可能含有的离子如表所示:| 可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
| Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
| n (Cl-) | 2.5mol | 3.0mol | 4.0mol |
| n (Br-) | 3.0mol | 2.6mol | 1.6mol |
| n (I-) | x mol | 0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③⑤①② | C. | ②①③⑤ | D. | ①⑤③② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L | |
| C. | NO2和N2O4 的混合气体中,NO2的体积分数是80% | |
| D. | 该合金中铜与镁的物质的量之比是2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
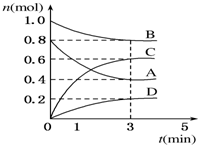 T℃时,在容积为0.5L的密闭容器中发生如 下反应.mA(g)+nB(g)?pC(g)+qD(s)△H<0(m、n、p、q为最简整数比).A、B、C、D的物质的量变化如图所示.
T℃时,在容积为0.5L的密闭容器中发生如 下反应.mA(g)+nB(g)?pC(g)+qD(s)△H<0(m、n、p、q为最简整数比).A、B、C、D的物质的量变化如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com