
(1)甲醇蒸气转化为氢气的一种原理是CH3OH和H2O反应生成CO2和H2。
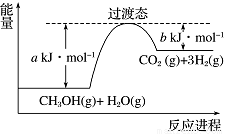
下图是该过程中能量变化示意图。若在反应体系中加入催化剂,反应速率增大,正反应活化能a的变化是___________(填“增大”、“减小”或“不变”),反应热ΔH的变化是________(填“增大”、“减小”或“不变”)。请写出反应进程CH3OH(g)和H2O(g)反应的热化学方程式___________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
已知:①CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
②2CO(g)+2NO(g)=N2(g)+2C O2(g) ΔH=-bkJ·mol-1(b>0)
O2(g) ΔH=-bkJ·mol-1(b>0)
若用标准状况下4.48 L CO还原NO2至N2(CO完全反应),整个过程中转移电子的物质的量为________,放出的热量为________kJ(用含有a和b的代数式表示)。
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:选择题
A、B、C、D四种物质均易溶于水(均不与水反应),分别按下列条件配成溶液,其中物质的量浓度最大的是 ( )
A.10 mL 5mol·L-1的A溶液加水配制成100 mL溶液
B.9.2 g B物质(相对分子质量为46)溶于水配成100 mL溶液
C.1.806×1023个C的分子溶于水配成100 mL溶液
D.0.1 moL D物质溶于100 mL 2.5 mol·L-1的D溶液中
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:选择题
在物质分类中,前者包括后者的是( )
A.氧化物、化合物 B.化合物、电解质
C.溶液、 胶体 D.置换反应、氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上学期期中化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.氧化还原反应中,一种元素被氧化,一定是另一种元素被还原
B.某元素由化合态变成游离态,此元素可能被氧化,也可能被还原
C.金属单质在反应中只能作 还原剂,非金属单质只能作氧化剂
还原剂,非金属单质只能作氧化剂
D.金属原子失电子越多,其还原性越强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上学期期中化学试卷(解析版) 题型:选择题
某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀盐酸,沉淀不溶解,则该溶液中
A.一定有SO42- B.可能有SO42- 或Ag+ C.一定无Ag+ D.还可能有CO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上学期期中化学试卷(解析版) 题型:选择题
常 温下某溶液中,由水电离出的c(H+)为1×10-12mol/L,该溶液中一定能大量共存的离子组是( )
温下某溶液中,由水电离出的c(H+)为1×10-12mol/L,该溶液中一定能大量共存的离子组是( )
A.K+、Na+、S2-、CO32- B. Na+、K+、SO42-、NO3-
Na+、K+、SO42-、NO3-
C.Fe2+、Mg2+、Cl-、SO42- D.NH4+、Cl-、K+、SO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二上学期期中化学试卷(解析版) 题型:选择题
下列措施能明显增大原反应的化 学反应速率的是( )
学反应速率的是( )
A.恒温恒容条件下,在工业合成氨反应中,增加氮气的量
B.将稀硫酸改为98%的浓硫酸与Zn反应制取 H2
H2
C.在H2SO4与NaOH两溶液反应时,增大压强
D.Na与水反应时增大水的用量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高二上学期期中化学试卷(解析版) 题型:选择题
已知25 ℃时,几种弱酸的电离常数如下:
弱酸的化学式 | CH3COOH | HCN | H2S |
电离常数 | 1.8×10-5 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
25 ℃时,下列说法正确的是( )
A.用0.1mol/LNaOH溶液滴定pH值相等CH3COOH和HCN溶液,CH3COOH消耗的NaOH溶液体积更大
B.等物质的量浓度的各溶液pH关系为:pH(Na2S)>pH(NaCN) >pH(NaHS)>pH(CH3COONa)
C.NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)+c(H2S)
D.某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-d mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:填空题
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应 来合成甲醇(于固定容器中进行):2H2(g) + CO(g)
来合成甲醇(于固定容器中进行):2H2(g) + CO(g) CH3OH(g)
CH3OH(g)
(1)下表所列数据是该反应在不同温度下的化学平衡常数(K)
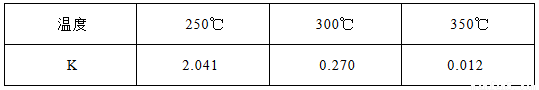
①该反应的熵变△S 0(填:“<,>,=”)。该反应在 (填:高温或低温)条件下能自发进行。
②要提高CO的转化率,可以采取的措施是_____________(填序号)。
a.升温
b.加入催化剂
c.增加CO的浓度
d.加入H2加压
e.加入惰性气体加压
f.分离出甲醇
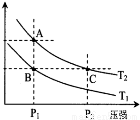
(2)如图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A__________C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A___________C,由状态B到状态A,可采用___________的方法(填“升温”或“降温”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com