
| A、1mol/L的AlCl3溶液 |
| B、2mol/L的NaCl溶液 |
| C、1.4mol/L的BaCl2溶液 |
| D、1mol/L的MgCl2溶液 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①③ |
| C、①③④⑤ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 历史上最早应用的还原性染料是靛蓝,其结构简式如图.下列关于靛蓝的叙述中错误的是( )
历史上最早应用的还原性染料是靛蓝,其结构简式如图.下列关于靛蓝的叙述中错误的是( )| A、靛蓝由碳、氢、氧、氮四种元素组成 |
| B、它的分子式是C16H10N2O2 |
| C、该物质苯环上的一溴代物有两种 |
| D、1mol靛蓝最多可与9mol氢气加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、5mL水 |
| B、10 mL 0.2 mol?L-1 MgCl2溶液 |
| C、20 mL 0.5 mol?L-1 NaCl溶液 |
| D、40mL 0.1 mo1?L-1盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
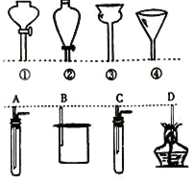 ①②③④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图(仪器中的药品及铁架台、铁夹等其它物品均已略去).请根据实际使用操作时上述漏斗的适用范围和它们的形状,指出A、B、C、D分别与①②③④中哪一种或哪几种最为匹配.A与
①②③④分别是几种常用漏斗的上部,A、B、C、D是实际应用操作(分液、制气、向容器中加液体试剂等)时,各种漏斗的下部插入容器中的示意图(仪器中的药品及铁架台、铁夹等其它物品均已略去).请根据实际使用操作时上述漏斗的适用范围和它们的形状,指出A、B、C、D分别与①②③④中哪一种或哪几种最为匹配.A与查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com