
 £¬øĆ·“Ó¦ĄąŠĶŹōÓŚĻūČ„·“Ó¦£®
£¬øĆ·“Ó¦ĄąŠĶŹōÓŚĻūČ„·“Ó¦£® £®
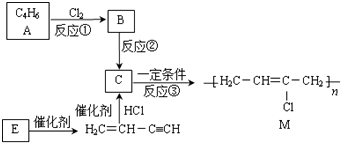
£®·ÖĪö ÓÉŗĻ³ÉĶ¼ŗĶMµÄ½į¹¹¼ņŹ½æÉÖŖCĪŖ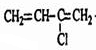 £¬·“Ó¦¢ŪĪŖ¼Ó¾Ū·“Ӧɜ³Éøß·Ö×Ó£»½įŗĻCµÄ½į¹¹æÉÖŖ£¬ÓÉAµÄ·Ö×ÓŹ½æÉÖŖ£¬AĪŖĮ“ד£¬Ó¦ŗ¬ÓŠ2øöC=CĖ«¼ü£¬ŌņAĪŖH2C=CH-CH=CH2£¬BĪŖH2C=CH-CH=CH2ÓėĀČĘų·¢Éś1£¬2-¼Ó³É²śĪļ£¬BĪŖ
£¬·“Ó¦¢ŪĪŖ¼Ó¾Ū·“Ӧɜ³Éøß·Ö×Ó£»½įŗĻCµÄ½į¹¹æÉÖŖ£¬ÓÉAµÄ·Ö×ÓŹ½æÉÖŖ£¬AĪŖĮ“ד£¬Ó¦ŗ¬ÓŠ2øöC=CĖ«¼ü£¬ŌņAĪŖH2C=CH-CH=CH2£¬BĪŖH2C=CH-CH=CH2ÓėĀČĘų·¢Éś1£¬2-¼Ó³É²śĪļ£¬BĪŖ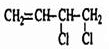 £¬ŌŚ¼īµÄ“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ӧɜ³ÉC£»ĄūÓĆĢāÖŠŠÅĻ¢£¬H2C=CH-C”ŌCHÓÉE¶ž¾ŪµĆµ½£¬ŌņEĪŖHC”ŌCH£¬Čż¾Ū»·×“²śĪļĪŖ±½”¢ĖľŪµĆµ½µÄ»·×“²śĪļĪŖ»·ŠĮĖÄĻ©£¬¼ų±š±½Óė»·ŠĮĖÄĻ©æÉÓĆäåĖ®£Ø±½·¢ÉśŻĶČ”¶ųŹ¹äåĖ®ĶŹÉ«”¢»·ŠĮĖÄĻ©ŌņÓėäå·¢Éś¼Ó³É·“Ó¦Ź¹äåĖ®ĶŹÉ«£©»ņĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£Ø±½²»ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«”¢»·ŠĮĖÄĻ©ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£©£¬¾Ż“Ė½ā“š£®
£¬ŌŚ¼īµÄ“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ӧɜ³ÉC£»ĄūÓĆĢāÖŠŠÅĻ¢£¬H2C=CH-C”ŌCHÓÉE¶ž¾ŪµĆµ½£¬ŌņEĪŖHC”ŌCH£¬Čż¾Ū»·×“²śĪļĪŖ±½”¢ĖľŪµĆµ½µÄ»·×“²śĪļĪŖ»·ŠĮĖÄĻ©£¬¼ų±š±½Óė»·ŠĮĖÄĻ©æÉÓĆäåĖ®£Ø±½·¢ÉśŻĶČ”¶ųŹ¹äåĖ®ĶŹÉ«”¢»·ŠĮĖÄĻ©ŌņÓėäå·¢Éś¼Ó³É·“Ó¦Ź¹äåĖ®ĶŹÉ«£©»ņĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£Ø±½²»ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«”¢»·ŠĮĖÄĻ©ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£©£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗÓÉŗĻ³ÉĶ¼ŗĶMµÄ½į¹¹¼ņŹ½æÉÖŖCĪŖ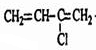 £¬·“Ó¦¢ŪĪŖ¼Ó¾Ū·“Ӧɜ³Éøß·Ö×Ó£»½įŗĻCµÄ½į¹¹æÉÖŖ£¬ÓÉAµÄ·Ö×ÓŹ½æÉÖŖ£¬AĪŖĮ“ד£¬Ó¦ŗ¬ÓŠ2øöC=CĖ«¼ü£¬ŌņAĪŖH2C=CH-CH=CH2£¬BĪŖH2C=CH-CH=CH2ÓėĀČĘų·¢Éś1£¬2-¼Ó³É²śĪļ£¬BĪŖ
£¬·“Ó¦¢ŪĪŖ¼Ó¾Ū·“Ӧɜ³Éøß·Ö×Ó£»½įŗĻCµÄ½į¹¹æÉÖŖ£¬ÓÉAµÄ·Ö×ÓŹ½æÉÖŖ£¬AĪŖĮ“ד£¬Ó¦ŗ¬ÓŠ2øöC=CĖ«¼ü£¬ŌņAĪŖH2C=CH-CH=CH2£¬BĪŖH2C=CH-CH=CH2ÓėĀČĘų·¢Éś1£¬2-¼Ó³É²śĪļ£¬BĪŖ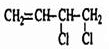 £¬ŌŚ¼īµÄ“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ӧɜ³ÉC£»ĄūÓĆĢāÖŠŠÅĻ¢£¬H2C=CH-C”ŌCHÓÉE¶ž¾ŪµĆµ½£¬ŌņEĪŖHC”ŌCH£¬Čż¾Ū»·×“²śĪļĪŖ±½”¢ĖľŪµĆµ½µÄ»·×“²śĪļĪŖ»·ŠĮĖÄĻ©£¬¼ų±š±½Óė»·ŠĮĖÄĻ©æÉÓĆäåĖ®£Ø±½·¢ÉśŻĶČ”¶ųŹ¹äåĖ®ĶŹÉ«”¢»·ŠĮĖÄĻ©ŌņÓėäå·¢Éś¼Ó³É·“Ó¦Ź¹äåĖ®ĶŹÉ«£©»ņĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£Ø±½²»ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«”¢»·ŠĮĖÄĻ©ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£©£¬
£¬ŌŚ¼īµÄ“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ӧɜ³ÉC£»ĄūÓĆĢāÖŠŠÅĻ¢£¬H2C=CH-C”ŌCHÓÉE¶ž¾ŪµĆµ½£¬ŌņEĪŖHC”ŌCH£¬Čż¾Ū»·×“²śĪļĪŖ±½”¢ĖľŪµĆµ½µÄ»·×“²śĪļĪŖ»·ŠĮĖÄĻ©£¬¼ų±š±½Óė»·ŠĮĖÄĻ©æÉÓĆäåĖ®£Ø±½·¢ÉśŻĶČ”¶ųŹ¹äåĖ®ĶŹÉ«”¢»·ŠĮĖÄĻ©ŌņÓėäå·¢Éś¼Ó³É·“Ó¦Ź¹äåĖ®ĶŹÉ«£©»ņĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£Ø±½²»ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«”¢»·ŠĮĖÄĻ©ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£©£¬
£Ø1£©ÓÉÉĻĆęµÄ·ÖĪöæÉÖŖ£¬AĪŖH2C=CH-CH=CH2£¬
¹Ź“š°øĪŖ£ŗH2C=CH-CH=CH2£»
£Ø2£©·“Ó¦¢ŚŹĒ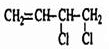 ŌŚ¼īµÄ“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ӧɜ³É
ŌŚ¼īµÄ“¼ČÜŅŗÖŠ·¢ÉśĻūČ„·“Ӧɜ³É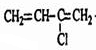 £¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ
£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»ĻūČ„£»
£»ĻūČ„£»
£Ø3£©ĄūÓĆĢāÖŠŠÅĻ¢H2C=CH-C”ŌCHÓÉE¶ž¾ŪµĆµ½£¬ŌņEĪŖHC”ŌCH£¬Čż¾Ū»·×“²śĪļĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø4£©1£¬4-¶”¶ž“¼£ØBDO£©ĪŖCH2OH-CH2CH2CH2OH£¬øł¾ŻAµÄ·Ö×ÓŹ½æÉÖŖAÓ¦ŗ¬ÓŠ2øöC=C£¬ÓėĀČĘųµÄ·“Ӧɜ³É1£¬4¼Ó³É£¬Éś³ÉCH2Cl-CH=CHCH2Cl£¬CH2Cl-CH=CHCH2ClŌŚ¼īŠŌĢõ¼žĻĀ·¢ÉśĖ®½ā£¬Éś³ÉCH2OH-CH=CHCH2OH£¬·“Ó¦µÄ·½³ĢŹ½ĪŖCH2Cl-CH=CHCH2Cl+2NaOH$”ś_{”÷}^{H_{2}O}$CH2OH-CH=CHCH2OH+2NaCl£¬CH2OH-CH=CHCH2OHÓėĒāĘų·¢Éś¼Ó³É·“Ó¦æÉÉś³ÉCH2OH-CH2CH2CH2OH£¬øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬Īåøö·“Ó¦¢Ł¢Ś¢Ū¢Ü¢ŻÖŠŹōÓŚČ”“ś·“Ó¦µÄŹĒ¢Ż£¬
¹Ź“š°øĪŖ£ŗCH2Cl-CH=CHCH2Cl+2NaOH$”ś_{”÷}^{H_{2}O}$CH2OH-CH=CHCH2OH+2NaCl£»¢Ż£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ»śĪļŗĻ³É£¬Ć÷Č·ĪļÖŹµÄ¹ŁÄÜĶż°ĘäŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬øł¾ŻĮ÷³ĢĶ¼¼°M½į¹¹²ÉÓĆÄęĻņĶʵ¼µÄ·½·Ø½ųŠŠĶʶĻ£¬ÖŖµĄ³£¼ūÓŠ»ś·“Ó¦ĄąŠĶ¼°·“Ó¦Ģõ¼ž£¬Ķ¬Ź±æ¼²éѧɜĮé»īŌĖÓĆÖŖŹ¶½ā“šĪŹĢāµÄÄÜĮ¦£¬ĪŖæ¼ŹŌČČµć£¬ĢāÄæÄѶČÖŠµČ£®


 ±¾ĶĮ½ĢøØÓ®ŌŚŹī¼Łøߊ§¼ŁĘŚ×Üø“Ļ°ŌĘÄĻæĘ¼¼³ö°ęÉēĻµĮŠ“š°ø
±¾ĶĮ½ĢøØÓ®ŌŚŹī¼Łøߊ§¼ŁĘŚ×Üø“Ļ°ŌĘÄĻæĘ¼¼³ö°ęÉēĻµĮŠ“š°ø Źī¼Ł×÷Ņµ±±¾©ŅÕŹõÓėæĘѧµē×Ó³ö°ęÉēĻµĮŠ“š°ø
Źī¼Ł×÷Ņµ±±¾©ŅÕŹõÓėæĘѧµē×Ó³ö°ęÉēĻµĮŠ“š°ø µŚČżŃ§ĘŚÓ®ŌŚŹī¼ŁĻµĮŠ“š°ø
µŚČżŃ§ĘŚÓ®ŌŚŹī¼ŁĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«1 mol Cl2ĶØČėµ½Ė®ÖŠ£¬ŌņN£ØHClO£©+N£ØCl-£©+N£ØClO-£©=2NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬3.0 gŗ¬¼×Č©µÄ±ł“×ĖįÖŠŗ¬ÓŠµÄŌ×Ó×ÜŹżĪŖ0.4NA | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24 LµÄCCl4ÖŠŗ¬ÓŠµÄC-Cl¼üŹżĪŖ0.4NA | |
| D£® | ½«CO2ĶعżNa2O2Ź¹ĘäŌöÖŲaæĖŹ±£¬·“Ó¦ÖŠ×ŖŅʵĵē×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 2015ÄźµÄĢģ½ņ±¬ÕØŹĀ¹ŹÖŠ£¬Ņņ±¬Õسå»÷µ¼ÖĀ²æ·Ö¾ē¶¾ĪļÖŹĒč»ÆÄĘ£ØNaCN£©Š¹Ā©£¬Õžø®³ÉĮ¢×ØĆÅ“¦ÖĆŠ”×飬ĶعżÅēČ÷Ė«ŃõĖ®»ņĮņ“śĮņĖįÄĘČÜŅŗĄ““¦Ąķ£¬ŅŌ¼õĒįĪŪČ¾£®
2015ÄźµÄĢģ½ņ±¬ÕØŹĀ¹ŹÖŠ£¬Ņņ±¬Õسå»÷µ¼ÖĀ²æ·Ö¾ē¶¾ĪļÖŹĒč»ÆÄĘ£ØNaCN£©Š¹Ā©£¬Õžø®³ÉĮ¢×ØĆÅ“¦ÖĆŠ”×飬ĶعżÅēČ÷Ė«ŃõĖ®»ņĮņ“śĮņĖįÄĘČÜŅŗĄ““¦Ąķ£¬ŅŌ¼õĒįĪŪČ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĶÖ¬Ė®½ā¾łæɵƵ½ĘĻĢŃĢĒ | B£® | æÉÓƵā¼ģŃéµķ·ŪŹĒ·ńĶźČ«Ė®½ā | ||
| C£® | µ°°×ÖŹĖ®½āæɵƵ½øß¼¶Ö¬·¾Ėį | D£® | ĻĖĪ¬ĖŲŌŚČĖŗĶ¶ÆĪļĢåÄŚ¶¼æÉĖ®½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆŹŌ¹Ü¼ÓČČĢ¼ĖįĒāÄĘ¹ĢĢåŹ±Ź¹ŹŌ¹ÜæŚŹśÖ±ĻņÉĻ | |
| B£® | Ź©·ŹŹ±£¬²ŻÄ¾»Ņ£ØÓŠŠ§³É·ÖĪŖK2CO3£©²»ÄÜÓėNH4Cl»ģŗĻŹ¹ÓĆ£¬ŹĒŅņĪŖK2CO3ÓėNH4Cl·“Ӧɜ³É°±Ęų»į½µµĶ·ŹŠ§ | |
| C£® | Na2CO3£Øs£©»ģÓŠNaHCO3£Øs£©Ź±æÉÓĆ×ĘÉյķ½·ØĢį“æ | |
| D£® | Š”ĖÕ“ņŹĒĆę°ü·¢½Ķ·ŪµÄÖ÷ŅŖ³É·Ö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | īčŹĒŅ×µ¼µēµÄŅų°×É«½šŹō | B£® | ÄÜÉś³É+3¼ŪµÄĄė×Ó»ÆŗĻĪļ | ||
| C£® | ÄÜÓėH+·“Ӧɜ³ÉH2 | D£® | Tl3+µÄŃõ»ÆŠŌ±ČAl3+Ēæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
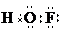 £¬ŌņHFOµÄ½į¹¹Ź½ĪŖ
£¬ŌņHFOµÄ½į¹¹Ź½ĪŖ £ØŌŚHFOµÄ½į¹¹Ź½ÖŠ±ź³öø÷ŌŖĖŲµÄ»ÆŗĻ¼Ū£©£®
£ØŌŚHFOµÄ½į¹¹Ź½ÖŠ±ź³öø÷ŌŖĖŲµÄ»ÆŗĻ¼Ū£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
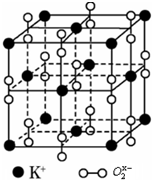 ČēĶ¼ŹĒ¼Ų”¢ŃõŌŖĖŲŠĪ³É¾§ĢåµÄŅ»øö¾§°ū£¬¾§ĢåÖŠŃõŌŖĖŲŅŌO2x-Ąė×ÓŠĪŹ½“ęŌŚ£®
ČēĶ¼ŹĒ¼Ų”¢ŃõŌŖĖŲŠĪ³É¾§ĢåµÄŅ»øö¾§°ū£¬¾§ĢåÖŠŃõŌŖĖŲŅŌO2x-Ąė×ÓŠĪŹ½“ęŌŚ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬ÅØĮņĖįæÉŅŌÓĆĀĮ¹Ž“¢“ę£¬ĖµĆ÷ĀĮÓėÅØĮņĖį²»·“Ó¦ | |
| B£® | Ź¢NaOHČÜŅŗµÄ²£Į§ŹŌ¼ĮĘæŠčÅäĻš½ŗČū£¬ĖµĆ÷²£Į§ÖŠµÄij³É·ÖÄÜÓė¼īŅŗ·“Ó¦ | |
| C£® | ÅØĻõĖį±£“ęŌŚ×ŲÉ«ŹŌ¼ĮĘæĄļ²¢ÖĆÓŚŅõĮ¹“¦£¬ĖµĆ÷ĻõĖįŹÜČČ»ņ¼ū¹āŅ×·Ö½ā | |
| D£® | ĻņµāĖ®ÖŠµĪ¼Ó±½£¬Õńµ“¾²ÖĆ·Ö²ć£¬±½²ć³Ź×ĻŗģÉ«£¬ĖµĆ÷æÉÓƱ½“ÓµāĖ®ÖŠŻĶČ”µā |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com