
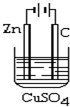
 电解原理在工业有广泛的应用.利用相关知识回答下面的问题.
电解原理在工业有广泛的应用.利用相关知识回答下面的问题.
| ||


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
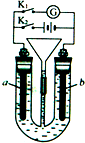 在如图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极.
在如图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极.查看答案和解析>>
科目:高中化学 来源: 题型:
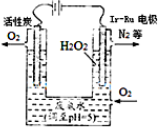 最近华南理工大提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图
最近华南理工大提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在NaHA溶液中一定有:c(Na+)>c(HA-)>c(OH-)>c(H+) |
| B、0.1mol/L(NH4)2Fe(SO4)2溶液中:c(SO42-)=c(NH4+)>c(Fe2+)>c(H+)>c(OH-) |
| C、0.2 mol?L-1CH3COOH溶液和0.2 mol?L-1CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol?L-1 |
| D、pH相等的①NH4Cl ②(NH4)2SO4③NH4HSO4溶液中,c (NH4+)大小顺序为①=②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
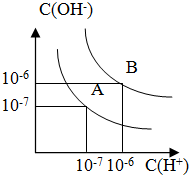 已知水在25℃和100℃时,其电离平衡曲线如图所示:
已知水在25℃和100℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验②证明Fe2+既有氧化性又有还原性 |
| B、实验③生成的气体不能使湿润的淀粉KI试纸变蓝 |
| C、上述实验中,有三个氧化还原反应 |
| D、上述实验证明氧化性:MnO2>MnO4->Cl2>Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com