
右图曲线a表示反应X(g)+Y(g) +N(s)  Z(g)+M(g) △H<0进行过程中X的转化
Z(g)+M(g) △H<0进行过程中X的转化
率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进
行,可采取的措施是( )
A.升高温度 B.加大N的投入量
C.缩小体积 D.加大X的投入量

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
分别用双线桥法和单线桥法分析下列氧化还原反应中化合价的变化,标出电子转移的方向和数目。
(1)2KNO3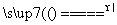 2KNO2+O2↑
2KNO2+O2↑
(2)Fe+H2SO4===FeSO4+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
VmL硫酸铁溶液中含wgSO42-,取此溶液0.5VmL,用水稀释成2VmL.则稀释后的溶液中Fe3+物质的量浓度为
A.125w/72v B.250w/72v C.250w/48v D.125w/18v
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应:X(g) + 3Y(g)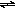 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol/L、0.3 mol/L、0.08 mol/L,下列判断不正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol/L、0.3 mol/L、0.08 mol/L,下列判断不正确的是( )
A.c1∶c2 =1∶3
B.平衡时,Y和Z生成速率之比为3∶2
C.X、Y的转化率不相等
D.c1的取值范围为0< c1< 0.14 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
依据氧化还原反应:
2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电
池,如图所示。请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________溶液。(填名称)
(2)银电极为电池的________极,发生的电极反应为____________________________;X电极上发生的电极反应为____________________________。
(3)外电路中的电子是从________极流向______极(填电极材料)。外电路中每通过0.1 mol电子,银电极的质量理论上增加 g。
(4)原电池工作时,盐桥(装有琼脂-KCl的U型管)里的Cl-移向 电极。
查看答案和解析>>
科目:高中化学 来源: 题型:
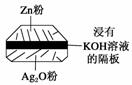
微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-。下列叙述正确的是( )
A.在使用过程中,电解质KOH被不断消耗
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.每转移2mol e-,有232gAg2O被氧化
D.Zn是负极,Ag2O是正极
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于叙述正确的是( )
A.室温下,浓度均为0.05mol/L的NaOH溶液和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12
B.室温下,将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,2c(SO42-)>c(NH4+)
C.室温下,0.1mol/L的盐酸和0.1mol/L的氢氧化钡等体积混合,混合后溶液pH=7
D.室温下,pH=4的醋酸溶液和pH=10的氢氧化钠溶液等体积混合后的溶液pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列溶液中,各组离子一定能够大量共存的是
A.含SCN-的溶液: Na+、Cl-、SO42-、Fe3+
B.使紫色石蕊试液变蓝的溶液:K+、Ba2+、Cl-、NO3-
C.-使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
D.碳酸氢钠溶液:K+、SO42-、Cl-、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.Na2O2可用于呼吸面具中氧气的来源
B.Na2O和Na2O2投入水中都能生成NaOH
C.Na2O2和Na2O均可以露置在空气中保存
D.NaCl的性质稳定,可用作调味品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com