
”¾ĢāÄæ”æ¹ŲÓŚNa2OŗĶNa2O2µÄŠšŹöÕżČ·µÄŹĒ£Ø””””£©
A.¶¼ŹĒ°×É«µÄ¹ĢĢå
B.¶¼ÄÜŗĶĖ®·“Ó¦ŠĪ³ÉĒæ¼īČÜŅŗ
C.¶¼ŹĒ¼īŠŌŃõ»ÆĪļ
D.ŃęÉ«·“Ó¦µÄŃÕÉ«¶¼ŹĒ×ĻÉ«
”¾“š°ø”æB
”¾½āĪö”æ½ā£ŗA”¢Na2OŹĒ°×É«¹ĢĢ壬Na2O2ŹĒµ»ĘÉ«¹ĢĢ壬ŃÕÉ«²»Ķ¬£¬¹ŹA“ķĪó£»
B”¢Na2OÓėNa2O2ÓėĖ®·“Ó¦¶¼ÄÜÉś³ÉĒāŃõ»ÆÄĘ£¬ĒāŃõ»ÆÄĘŹĒĒæ¼ī£¬¹ŹBÕżČ·£»
C”¢ŅņNa2O2ÓėĖį·“Ӧɜ³ÉŃĪ”¢Ė®ŗĶŃõĘų£¬ŌņNa2O2²»ŹōÓŚ¼īŠŌŃõ»ÆĪļ£¬¹ŹC“ķĪó£»
D”¢Na2OŗĶNa2O2ÖŠ¶¼ŗ¬ÓŠÄĘŌŖĖŲ£¬ĖłŅŌŃęÉ«·“Ó¦µÄŃÕÉ«¶¼ŹĒ»ĘÉ«£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®


 Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø
Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻÓŠ¹ŲÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā
£Ø1£©25”ꏱ£¬0.1 molL£1µÄŅ»ŌŖĖįHAČÜŅŗÖŠc(H£«)£½1.0”Į10£4 molL£1£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ“ĖŹ±ČÜŅŗµÄpH£½_______£¬HAŹĒ________Ėį£ØĢī”°Ēæ”±»ņ”°Čõ”±£©”£
£Ø2£©ĻÖÓŠNaHCO3”¢NaHSO3”¢NaHSO4ČżÖÖ³£¼ūµÄĖįŹ½ŃĪ£¬ĖüĆĒŌŚ¹¤ŅµÉś²śŗĶČÕ³£Éś»ī֊ӊ׏ć·ŗµÄÓ¦ÓĆ”£Ēė»Ų“šÓŠ¹ŲĪŹĢā£ŗ
¢Ł25”ꏱ£¬NaHCO3µÄĖ®ČÜŅŗĻŌ_____ŠŌ£ØĢī”°Ėį”±»ņ”°¼ī”±£©”£
¢Ś25”ꏱ£¬ĪļÖŹµÄĮæÅØ¶Č¾łĪŖ0.01 molL£1µÄČżÖÖĖįŹ½ŃĪČÜŅŗ£¬pH×īŠ”ŹĒ_________”£
£Ø3£©Ļņ50ml 0.018molL£1µÄAgNO3ČÜŅŗÖŠ¼ÓČė50m1 0.020molL£1µÄŃĪĖįÉś³ÉAgCl³Įµķ”£ŅŃÖŖøĆĪĀ¶ČĻĀKsp(AgCl)£½1.0”Į10©10£¬ŗöĀŌČÜŅŗµÄĢå»ż±ä»Æ£¬ĶźČ«³Įµķŗó£¬ČÜŅŗÖŠc(Ag+)£½__molL£1”£
£Ø4£©ÓĆĖįŠŌKMnO4ČÜŅŗµĪ¶Øŗ¬ŌÓÖŹµÄNa2C2O4ѳʷ£ØŌÓÖŹ²»²ĪÓė·“Ó¦£©”£
ŹµŃé²½Öč£ŗ×¼Č·³ĘČ”1g Na2C2O4¹ĢĢåѳʷ£¬ÅäÖĘ³É100mLČÜŅŗ£¬Č”³ö20.00mLӌ׶ŠĪĘæÖŠ”£ŌŁĻņ׶ŠĪĘæÖŠ¼ÓČė×ćĮæĻ”H2SO4ČÜŅŗ£¬ÓĆ0.016 molL£1øßĆĢĖį¼ŲČÜŅŗµĪ¶Ø£¬µĪ¶ØÖĮÖÕµćŹ±ĻūŗÄøßĆĢĖį¼ŲČÜŅŗ25.00mL”£
£ØŅŃÖŖ£ŗ5H2C2O4£«2KMnO4£«3H2SO4£½10CO2”ü£«2MnSO4£«K2SO4£«8H2O£©
¢ŁøßĆĢĖį¼ŲČÜŅŗӦװŌŚ_______µĪ¶Ø¹ÜÖŠ£®£ØĢī”°ĖįŹ½”±»ņ”°¼īŹ½”±£©”£
¢ŚµĪ¶ØÖĮÖÕµćŹ±µÄŹµŃéĻÖĻóŹĒ£ŗ__________________________________________”£
¢ŪĻĀĮŠ²Ł×÷æÉÄÜŹ¹²āĮæ½į¹ūĘ«øߵďĒ__________”£
A£®Ź¢×°µÄNa2C2O4µÄµĪ¶Ø¹ÜĆ»ČóĻ“
B£®Ź¢×°øßĆĢĖį¼ŲČÜŅŗµÄµĪ¶Ø¹ÜµĪ¶ØĒ°¼ā×ģ“¦ÓŠĘųÅŻ£¬µĪ¶ØŗóĘųÅŻĻūŹ§
C£®¶ĮŹżŹ±µĪ¶ØĒ°ŃöŹÓ£¬µĪ¶Øŗóø©ŹÓ
D£®×¶ŠĪĘæÖŠ²ŠĮōÉŁĮæĖ®
¢Ü¼ĘĖćѳʷ֊Na2C2O4µÄ“æ¶Č______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25”ꏱ£¬ÓŠc(CH3COOH)+c(CH3COO-)=0.1mol”¤L-1µÄŅ»×é“×Ėį”¢“×ĖįÄĘ»ģŗĻČÜŅŗ£¬ČÜŅŗÖŠc(CH3COOH)”¢c(CH3COO-)¶žÕßĖłÕ¼ĪļÖŹµÄĮæ·ÖŹż(a)ĖęČÜŅŗpH±ä»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
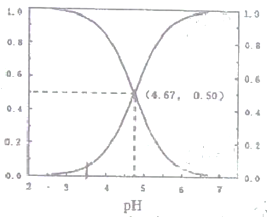
A. pH£¼4.67µÄČÜŅŗÖŠ£ŗc(CH3COO-)£¼c(CH3COOH)
B. pH=7µÄČÜŅŗÖŠ£ŗc(CH3COOH)=0£¬c(CH3COO-)=1.0
C. ŌŚpH=4.67µÄČÜŅŗÖŠ£ŗc(Na+)+c(H+)=c(CH3COOH)+c(0H-)
D. pH=3.5µÄČÜŅŗÖŠ£ŗc(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol”¤L-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠNaCl”¢FeCl2”¢FeCl3”¢MgCl2”¢AlCl3ĪåÖÖČÜŅŗ£¬Ö»ÓĆŅ»ÖÖŹŌ¼Į¾ĶæÉŅŌ¼ų±šĖüĆĒ£¬ÕāÖÖŹŌ¼ĮŹĒ£Ø””””£©
A.ŃĪĖį
B.NaOHČÜŅŗ
C.°±Ė®
D.KSCNČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææŲÖĘŹŹµ±µÄĢõ¼ž£¬½«·“Ó¦2Fe3++2I-![]() 2Fe2++I2Éč¼Ę³ÉČēĶ¼ĖłŹ¾µÄŌµē³Ų£¬ĻĀĮŠÅŠ¶Ļ“ķĪóµÄŹĒ
2Fe2++I2Éč¼Ę³ÉČēĶ¼ĖłŹ¾µÄŌµē³Ų£¬ĻĀĮŠÅŠ¶Ļ“ķĪóµÄŹĒ
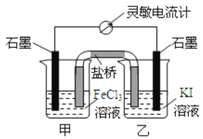
A. ·“Ó¦æŖŹ¼Ź±£¬ŅŅÖŠµē¼«·“Ó¦ĪŖ2I--2e-=I2
B. ·“Ó¦æŖŹ¼Ź±£¬¼×ÖŠŹÆÄ«µē¼«ÉĻ·¢Éś»¹Ō·“Ó¦
C. µēĮ÷¼Ę¶ĮŹżĪŖĮ揱£¬·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬
D. Ę½ŗāŹ±ŅŅÖŠČÜČėµāŗ󣬼׳ŲµÄŹÆÄ«µē¼«ĪŖÕż¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ»śĪļµÄ·Ö×ÓÖŠ£¬²»æÉÄÜĖłÓŠŌ×Ó¾ł¹²Ę½ĆęµÄŹĒ
A. ŅŅĶé B. ŅŅĻ© C. ±½ D. ŅŅČ²
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĘū³µ¾ēĮŅÅöײŹ±£¬°²Č«ĘųÄŅÖŠ·¢Éś·“Ó¦10NaN3+2KNO3= K2O+5Na2O+16N2”ü£¬¶ŌÓŚøĆ·“Ó¦£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
A. NaN3ÖŠµŖŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ-3
B. Ńõ»Æ¼ĮŗĶ»¹Ō¼ĮŹĒĶ¬Ņ»ĪļÖŹ
C. ±»Ńõ»ÆµÄµŖŌ×ÓÓėÉś³ÉµÄµŖĘų·Ö×ÓøöŹżÖ®±ČĪŖ15:8
D. ·“Ó¦¹ż³ĢÖŠČō×ŖŅĘ1molµē×Ó£¬Ōņ²śÉś2.24LĘųĢå£Ø±ź×¼×“æö£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠÓÉĮ½ÖÖ½šŹōŌŖĖŲ×é³ÉµÄŗĻ½š10.5g£¬Ķ¶Čė×ćĮæµÄĻ”ĮņĖįÖŠ·“Ó¦ĶźČ«ŗ󣬲āµĆÉś³ÉĒāĘų1g£¬Ōņ×é³ÉøĆŗĻ½šµÄŌŖĖŲæÉÄÜŹĒ
A. FeÓėZn B. MgÓėCu C. NaÓėMg D. AlÓėFe
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬ÓĆĖ®Ļ”ŹĶ0.1 mol/LµÄ“×ĖįČÜŅŗ£¬Ėę¼ÓĖ®ĮæµÄŌö¼Ó¶ųŌö“óµÄŹĒ( )
A£®n(CH3COOH) B£®c(H+) C£® c(H+) ”¤c(OH-) D£® c(H+)/c(CH3COOH)
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com