
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
现有pH=2的醋酸甲和pH=2的盐酸乙:
(1)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡________(填“向左”、“向右”或“不”)移动;若加入少量的冰醋酸,醋酸的电离平衡________(填“向左”、“向右”或“不”)移动,若加入少量无水醋酸钠固体,待固体溶解后,溶液中c(H+)/c(CH3COOH)的值将________(填“增大”、“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为pH(甲)________(填“大于”、“小于”或“等于”)pH(乙)。若将甲、乙两溶液等体积混合,溶液的pH=__________。
(3)各取25 mL的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和至pH=7,则消耗的NaOH溶液的体积大小关系为V(甲)________(填“大于”、“小于”或“等于”)V(乙)。
(4)取25 mL的甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中c(Na+)、c(CH3COO-)的大小关系为c(Na+)________(填“大于”、“小于”或“等于”)c(CH3COO-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是( )
A.SO2和SiO2 B.CO2和H2O
C.NaCl和HCl D.CCl4和KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2CH3COCH3(l)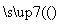 CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0 ℃和20 ℃下,测得其转化分数Y随时间t变化的关系曲线(Y—t)如图所示。下列说法正确的是( )
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0 ℃和20 ℃下,测得其转化分数Y随时间t变化的关系曲线(Y—t)如图所示。下列说法正确的是( )
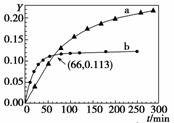
A.b代表0 ℃下CH3COCH3的Y—t曲线
B.反应进行到20 min末,CH3COCH3的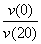 >1
>1
C.升高温度可缩短反应达平衡的时间并提高平衡转化率
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的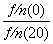 =1
=1
查看答案和解析>>
科目:高中化学 来源: 题型:
用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。
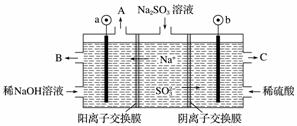
(1)图中a极要连接电源的________(填“正”或“负”)极,C口流出的物质是________。
(2)SO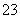 放电的电极反应式为____________。
放电的电极反应式为____________。
(3)电解过程中阴极区碱性明显增强,用平衡移动原理解释原因________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)所有金属纯度越大,越不易被腐蚀( )
(2)纯银器表面变黑和钢铁表面生锈腐蚀原理一样( )
(3)干燥环境下金属不被腐蚀( )
(4)Al、Fe、Cu在潮湿的空气中腐蚀均生成氧化物( )
(5)钢铁发生电化学腐蚀时,负极铁失去电子生成Fe3+( )
(6)在金属表面覆盖保护层,若保护层破损后,就完全失去了对金属的保护作用( )
(7)外加电流的阴极保护法,构成了电解池;牺牲阳极的阴极保护法构成了原电池。二者均能有效地保护金属不容易被腐蚀( )
查看答案和解析>>
科目:高中化学 来源: 题型:
有关金属的腐蚀与防护的叙述正确的是( )
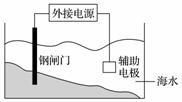
A.金属的化学腐蚀比电化学腐蚀普遍
B.上图装置的原理是“牺牲阳极的阴极保护法”
C.金属腐蚀的本质是M-ne-===Mn+而被损耗
D.用铝质铆钉来接铁板,铁板易被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
要证明某溶液中不含Fe3+而可能含有Fe2+进行如下实验操作时,最佳顺序为( )
①加入足量氯水 ②加入足量酸性KMnO4溶液 ③加入少量NH4SCN溶液
A.①③ B.③② C.③① D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com