
| A. | 精铜板作阴极,纯铜片作阳极,CuSO4溶液作电解液 | |
| B. | 电解时,阴极发生氧化反应,则阴极发生的反应为:Cu2++2e-═Cu | |
| C. | 粗铜中所含Ni、Fe、Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥 | |
| D. | 电解铜的纯度可达99.95%~99.98% |
分析 电镀法精炼铜时,粗铜为阳极,精铜为阴极,阳极材料是粗铜,阳极上金属失电子变成离子进入溶液,Cu-2e-=Cu2+,比金属铜活泼的金属锌、铁、镍会先于金属铜失电子,比金属铜活泼性差的Pt、Ag等固体会沉积下来形成阳极泥,这样最终电解铜的纯度可达99.95%~99.98%,以此解答该题.
解答 解:A.电镀法精炼铜时,粗铜为阳极,纯铜为阴极,电解质为硫酸铜,故A错误;
B.电解时,阳极上只要是金属Cu失电子变成离子进入溶液,Cu-2e-=Cu2+,阳极发生氧化反应,故B错误;
C.粗铜中所含Pt、Au、Ag等金属杂质,电解后以单质形式沉积槽底,形成阳极泥,金属镍、铁都比铜活泼,先于金属铜失电子,故C错误;
D.阴极只有铜离子得到电子,电解铜的纯度可达99.95%~99.95%,故D正确.
故选D.
点评 本题考查电解原理及应用,为高频考点,把握粗铜精炼的原理、电极反应为解答的关键,侧重分析与应用能力的考查,注意阳极泥的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 小苏打可用作糕点的膨化剂 | |
| B. | “地沟油“经过加工处理可用来制肥皂 | |
| C. | 多地花重金购买“雾霾消除车“,从根本上缓解了雾霾问题 | |
| D. | 装饰材料释放的苯、甲苯、甲醛等易挥发性物质会导致室内空气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
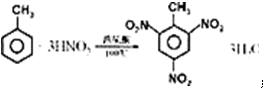 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
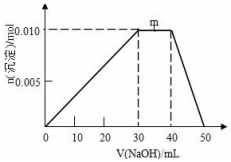 向盛有10mL1mol•L-1 NH4Al(SO4)2溶液的烧杯中滴加1mol•L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
向盛有10mL1mol•L-1 NH4Al(SO4)2溶液的烧杯中滴加1mol•L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在空气质量日报中CO2含量属于空气污染指数 | |
| B. | 日常生活中和医院常用无水乙醇杀菌消毒 | |
| C. | 绿色食品是指不含任何化学物质的食品 | |
| D. | 目前加碘食盐中主要添加的是KIO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
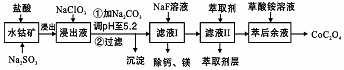
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
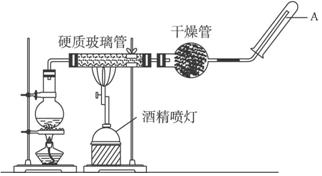 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性强弱HIO4<HBrO4<HClO4 | B. | 原子半径大小S>Na>O | ||
| C. | 碱性强弱KOH<NaOH<LiOH | D. | 金属性强弱Na<Mg<Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com