
【题目】下列物质中,属于酸的是
A.Na2OB.NaOHC.MgCl2D.H2SO4
 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 78gNa2O2固体中含有的离子数之和为3NA
B. 标准状况下22.4LCl2通入足量水中,反应中转移的电子数为NA
C. 18gD2O所含有的质子数、电子数均为10NA
D. pH=1的醋酸溶液中含有的H+数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组进行如下实验测定 H2C2O4·xH2O 中 x 值已知:M(H2C2O4)=90gmol-1
① 称取1.260 g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液;
② 取25.00 mL 待测液放入锥形瓶中,再加入适量的稀 H2SO4;
③ 用浓度为 0.05 000 mol·L-1 的 KMnO4标准溶液进行滴定。
(1)请写出滴定中发生反应的离子方程式________________________。
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是_____(选填 a、b)。
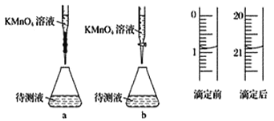
(3)由图可知消耗 KMnO4 溶液体积为________mL。
(4)滴定过程中眼睛应注视_______________,滴定终点锥形瓶内溶液的颜色变化为_______。
(5)通过上述数据,求得 x=_____。
a.若由于操作不当,滴定结束后滴定管尖嘴处有一气泡, 引起实验结果_____(填“偏大”、“偏小”或“无影响”);
b.若在接近终点时,用少量蒸馏水将锥形瓶冲洗一下,再继续滴定至终点,则所测结果_______(填“偏大”、“偏小”或“无影响”);
c.若在达到滴定终点时仰视读数,则所得结果________(填“偏大”、“偏小”或“无影响”);
d.若其它操作均正确,滴定前未用标准 KMnO4 溶液润洗滴定管,引起实验结果_________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PX是纺织工业的基础原料,其结构简式如下,下列说法正确的是( )
![]()
A. PX的一氯代物有3种 B. PX的分子式为C8H10
C. PX与乙苯互为同系物 D. PX分子中所有原子都处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯乙烯b、立方烷d、环辛四烯p的分子式均为C8H8,下列说法正确的是( )
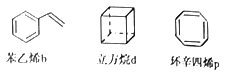
A. b、p中的所有原子可能处于同一平面 B. b、d的二氯代物均只有三种
C. b、p均不可与酸性高锰酸钾溶液反应 D. b的同分异构体只有d和p两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸的电离方程式为CH3COOH(aq)![]() H+(aq)+CH3COO-(aq) ΔH>0。25℃时,0.1mol/L醋酸溶液中存在下述关系:Ka=c(H+).c(CH3COO-)/c(CH3COOH)=1.75×10-5,其中的数值是该温度下醋酸的电离平衡常数(Ka)。下列说法正确的是
H+(aq)+CH3COO-(aq) ΔH>0。25℃时,0.1mol/L醋酸溶液中存在下述关系:Ka=c(H+).c(CH3COO-)/c(CH3COOH)=1.75×10-5,其中的数值是该温度下醋酸的电离平衡常数(Ka)。下列说法正确的是
A. 向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小
B. 向该溶液中加少量CH3COONa固体,平衡正向移动
C. 该温度下0.01mol/L醋酸溶液Ka<1.75×10-5
D. 升高温度,c(H+)增大,Ka变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中通入一定量的HI气体,使其在一定条件下发生反应:2HI(g)![]() H2(g)+I2(g)。下列叙述中,一定属于平衡状态的是
H2(g)+I2(g)。下列叙述中,一定属于平衡状态的是
A. HI、H2、I2的浓度相等
B. 混合气体的颜色不再变化
C. 混合气体的总压强不再变化
D. v(HI)∶v(H2)∶v(I2)=2∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期主族元素的原子序数依次增大。X、Y原子的最外层电子数之比为2∶3,Z+与Y2-核外电子排布完全相同,常温下,W的一种单质为淡黄色固体。下列说法不正确的是( )
A. 离子半径:W>Z>Y
B. 简单气态氢化物的热稳定性:Y>W
C. Y分别与X、Z、W能形成两种或两种以上的化合物
D. Z与Y、W分别形成的化合物溶于水,溶液均呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是( )
A. 原子半径由小到大的顺序:X< Y < Z< W
B. Z的最高价氧化物能与水反应生成相应的酸
C. Y单质在一定条件下可以与氧化铁发生置换反应
D. X、Z的氧化物形成的晶体类型相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com