
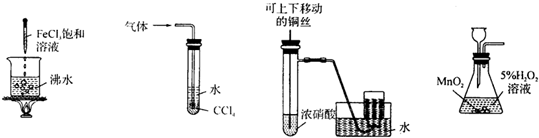
| A. | 得到红褐色沉淀 | B. | 吸收氨气,并防止倒吸 | ||
| C. | 制备并收集少量NO2气体 | D. | 实验室制O2 |
分析 A.胶体不是沉淀;
B.有缓冲装置的能防止倒吸;
C.二氧化氮能和水反应生成硝酸和NO;
D.应该用分液漏斗盛放双氧水.
解答 解:A.将氯化铁饱和溶液滴入沸水中,加热至溶液呈红褐色为止得到胶体,胶体不是沉淀,故A错误;
B.有缓冲装置的能防止倒吸,氨气不易溶于四氯化碳且和四氯化碳不反应,所以该装置有缓冲作用,能防止倒吸,故B正确;
C.二氧化氮能和水反应生成硝酸和NO,应该用向上排空气法收集,故C错误;
D.应该用分液漏斗盛放双氧水,否则产生的气体从长颈漏斗中逸出,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及物质制备、气体收集、尾气处理等知识点,明确实验原理、物质性质及实验基本操作是解本题关键,侧重考查学生实验操作能力,会根据气体溶解性及密度确定气体收集方法,题目难度不大.


科目:高中化学 来源: 题型:解答题
| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c[NH3•H2O] | B. | c[H+] | C. | c[OH-] | D. | c[NH4+] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多 | |
| B. | 第二周期元素从Li到F,金属性逐渐减弱,非金属性逐渐增强 | |
| C. | 因为Na比K容易失去电子,所以Na比K的还原性强 | |
| D. | O与S为同主族元素,且O比S的非金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
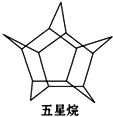 化学家合成了一种新物质-五星烷,它的分子立体结构如图所示:
化学家合成了一种新物质-五星烷,它的分子立体结构如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物在熔融态时不能导电 | |
| B. | 氢键是一种化学键,且它比分子间作用力要稍强 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 双原子分子中的共价键一定是非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
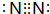 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com