
分析 (1)太阳能是取之不尽用之不竭的能源;
(2)利用热化学方程式和盖斯定律计算所需热化学方程式,三式相加得;
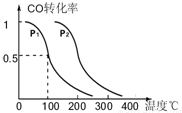
(3)根据定一议二原则,相同温度下,同一容器中,增大压强,平衡向正反应方向移动,则CO的转化率增大;
相同压强下,同一容器中,增大温度,CO的转化率减小,平衡向吸热反应方向移动,由此判断.
解答 解:(1)太阳光是取之不尽用之不竭的能源,故C最节能,故答案为:C;
(2)利用盖斯定律进行计算,将三个方程式进行形式变换,
2CO(g)+4H2(g)=2CH3OH(g)△H=-181.4 kJ•mol-1
2CH3OH(g=CH3OCH3(g)+H2O(g)△H=-23.5 kJ•mol-1
2CO2(g)+2H2(g)=2CO(g)+2H2O(g)△H=+82.4 kJ•mol-1
三式相加得:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)△H=-122.5 kJ•mol-1,
故答案为:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)△H=-122.5 kJ•mol-1;
(3)相同温度下,同一容器中,增大压强,平衡向正反应方向移动,则CO的转化率增大,根据图象知,p1小于p2,相同压强下,同一容器中,增大温度,CO的转化率减小,平衡向吸热反应方向移动,所以逆反应为吸热方向,则正反应为放热反应,所以△H<0,
故答案为:<;<.
点评 本题考查盖斯定律的应用,化学平衡移动的影响因素及读图能力,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均变性了 |
| B | 将淀粉溶液和稀H2SO4混合加热后,再滴加新制的Cu(OH)2悬浊液,煮沸 | 无砖红色沉淀产生 | 淀粉未水解 |
| C | 向苯酚浓溶液中滴加少量溴水,振荡 | 无白色沉淀 | 苯酚与溴水不反应 |
| D | CH3COOH、C2H5OH和浓H2SO4共热制备CH3COOC2H5,将共热后产生的气体导入盛有饱和Na2CO3溶液的试管中 | 有油状物浮于Na2CO3溶液表面,振荡后,油状层变薄 | 证明油状物不全部是CH3COOC2H5 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | Cl-Cl | Br-Br | I-I | H-Cl | H-Br | H-I | H-H |
| 键能(kJ/mol) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
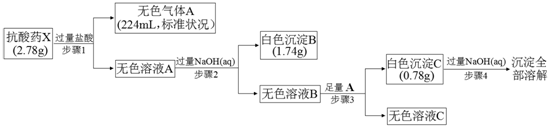
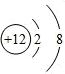 ,A的电子式为
,A的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保存氢氧化钠溶液、硅酸钠溶液等碱性试剂,常用带橡胶塞的玻璃瓶 | |
| B. | 保存浓硝酸及硝酸银溶液,常用带玻璃塞的棕色试剂瓶 | |
| C. | 保存金属钠和液溴时,常在试剂瓶中加入煤油进行封存 | |
| D. | 保存氢氟酸时,常用塑料瓶而不用玻璃瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定产生BaSO4沉淀 | B. | 一定产生BaSO3沉淀 | ||
| C. | 一定没有SO2逸出 | D. | 一定有SO3逸出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com