
【题目】已知反应①:CO(g)+CuO(s)![]() CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)![]() Cu(s)+H2O(g)在相同的温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
A.反应①的平衡常数K1=[c(CO2)c(Cu)]/[c(CO)c(CuO)]
B.对于反应③,恒容时,温度升高,H2的浓度减小,则该反应的焓变为正值
C.反应③的平衡常数K=K1/K2
D.对于反应③,恒温恒容下,增大压强,H2的浓度一定减小
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】
I.某化学兴趣小组对下列三组物质进行研究:
A.HCl、H2SO4、H2CO3、HNO3
B.溶液、水、悬浊液、胶体
C.Na2CO3、NaNO3、AgNO3、Ba(NO3)2
请你帮他们完善下列空白:
A | B | C | |
分类标准 | 含氧酸 | 分散系 | (3) |
不属于该类别的物质 | (1) | (2) | Na2CO3 |
II.“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
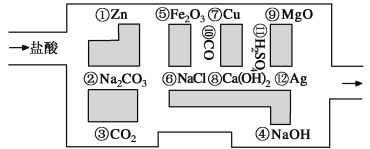
(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线):________________。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有________个,其中能“吃掉”盐酸的盐是____________,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,是氯碱工业的主要产品之一,它是一种常用的消毒剂。
①实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是______________________
②氯碱工业生产氯气的化学方程式为______________________
③由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是______________________,在空气中漂白粉长期存放会变质而失效的原理是(用化学方程式说明) _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方案中,括号内为除去杂质所需的药品,其中正确的是
A.NaOH溶液中混有Ba(OH)2(CuSO4) B.Cu(NO3)2溶液中混有AgNO3(Cu粉)
C.氧化铜中混有少量的铜粉(稀硫酸) D.NaCl溶液中混有BaCl2(CO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积均为1 L密闭容器中以不同的氢碳比[n(H2)/n(CO2)]充入H2和CO2,在一定条件下发生反应:2CO2(g)+ 6H2 (g)![]() C2H4(g)+ 4H2O(g)ΔH。CO2的平衡转化率α(CO2)与温度的关系如下图所示。下列说法正确的是( )
C2H4(g)+ 4H2O(g)ΔH。CO2的平衡转化率α(CO2)与温度的关系如下图所示。下列说法正确的是( )

A.该反应的ΔH > 0
B.氢碳比:X < 2.0
C.在氢碳比为2.0时,Q点v(逆)小于P点的v(逆)
D.P点温度下,反应的平衡常数为512
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图所示装置进行实验,若x轴表示流入阴极的电子的物质的量,则y轴应表示( )

①c(Ag+) ②c(NO![]() ) ③a棒的质量
) ③a棒的质量
④b棒的质量 ⑤c(H+)
A.①③ B.③④ C.①②④ D.①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,B是地壳中含量最高的金属元素,C单质的晶体是良好的半导体材料,D的最外层电子数与内层电子数之比为3:5。
(1)C的原子结构示意图为 ,D在元素周期表中的位置 。
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为 ;A单质在E单质中燃烧生成化合物乙,乙的电子式为 。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为 。
(4)含B元素的化合物常用作净水剂,用文字和化学用语解释净水原因: 。
(5)E元素的非金属性强于D元素,用原子结构解释原因:同周期元素随着原子序数递增, ,非金属性增强。
(6)工业上将干燥的E单质通人D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com