
| A. | 氯水能导电,所以氯气是电解质 | |
| B. | 氯化钙溶液在电流作用下电离出Ca2+和Cl- | |
| C. | 易溶于水的化合物一定是强电解质 | |
| D. | 硝酸钠在水中的电离方程式为NaNO3═Na++NO3- |
科目:高中化学 来源: 题型:解答题
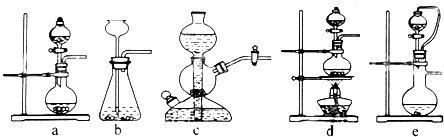
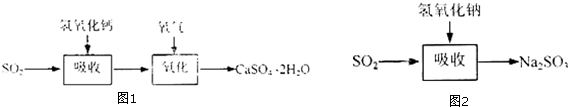
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,硫酸溶液的导电能力应强于醋酸溶液的导电能力 | |
| B. | NaCl在电流作用下电离成Na+和Cl- | |
| C. | CuSO4溶液导电时要伴随化学变化 | |
| D. | CO2水溶液的导电能力较弱,CO2是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3溶于水后能导电,故SO3为电解质 | |
| B. | 在蒸馏水中滴加浓H2SO4,KW不变 | |
| C. | CaCO3难溶于稀硫酸,也难溶于醋酸 | |
| D. | KCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
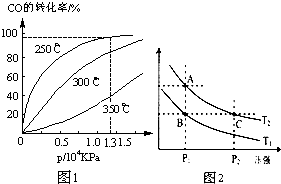 工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:
工业上一般在恒容密闭容器中可以采用下列反应合成甲醇:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | OH-、NO3-、HCO3-、Na+ | B. | Na+、SO42-、Mg2+、I- | ||
| C. | NO3-、Cu2+、K+、Cl- | D. | H+、K+、ClO-、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
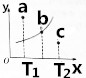 某温度下的2L密闭容器中发生某一特定反应,3中气体起始状态和平衡状态时的物质的量(n)如下表所示,2s时达到平衡状态.回答下列问题:
某温度下的2L密闭容器中发生某一特定反应,3中气体起始状态和平衡状态时的物质的量(n)如下表所示,2s时达到平衡状态.回答下列问题:| 密闭容器 | A | B | C |
| n(起始状态)/mol | 4 | 2 | 0 |
| n(平衡状态)/mol | 2.8 | 1.4 | 1.2 |
| 密闭容器 | 甲 | 乙 | 丙 | 丁 | |
| 密闭容器体积/L | 2 | 2 | 2 | 1 | |
| 起始物质的量 | n(A)/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n(B)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| A的平衡转化率 | 80 | α1 | α2 | α3 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com