
(6分)按要求填空:
(1)Fe(OH)2在空气中变质的化学方程为:_____________________________。
(2)漂白粉在空气中久置会变质,变质过程中既有非氧化还原反应又有氧化还原反应,其中氧化还原反应的方程式为:_______________________________。
(3)实验室制备氨气的反应方程式为:______________________,收集氨气时,在试管口放一小团棉花其作用是________________,用_______________试纸检验氨气是否收集满。
(4)将CaMg3Si4O12改写为氧化物的形式:_______________________。
(每空1分,共6分) (1)4Fe(OH)2+O2+2H2O=4Fe(OH)3 (2)2HClO 2HCl+O2↑
2HCl+O2↑
(3)2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O 防止与空气对流 湿润的红色石蕊试纸(不写湿润不给分) (4)CaO·3MgO·4SiO2
CaCl2+2NH3↑+2H2O 防止与空气对流 湿润的红色石蕊试纸(不写湿润不给分) (4)CaO·3MgO·4SiO2
【解析】
试题分析:(1)氢氧化亚铁易被氧气氧化为氢氧化铁,则Fe(OH)2在空气中变质的化学方程为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(2)漂白粉中的次氯酸钙能吸收空气中的水蒸气和CO2生成次氯酸和碳酸钙,该反应是复分解反应,不是氧化还原反应,反应的化学方程式为Ca(ClO)2+CO2+H2O=2HClO+CaCO3↓。生成的次氯酸不稳定见光易分解生成氯化氢和氧气,该反应是氧化还原反应,方程式为2HClO 2HCl+O2↑。
2HCl+O2↑。
(3)实验室制备氨气的反应方程式为2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O。由于氨气的密度比空气小,需要用向下排空气法收集,因此收集氨气时,在试管口放一小团棉花其作用是防止与空气对流;氨气是碱性气体,能使湿润的红色石蕊试纸变蓝色,所以用湿润的红色石蕊试纸检验氨气是否收集满。
CaCl2+2NH3↑+2H2O。由于氨气的密度比空气小,需要用向下排空气法收集,因此收集氨气时,在试管口放一小团棉花其作用是防止与空气对流;氨气是碱性气体,能使湿润的红色石蕊试纸变蓝色,所以用湿润的红色石蕊试纸检验氨气是否收集满。
(4)用氧化物形式表述硅酸盐时,一般活泼的金属氧化物在前,最后是二氧化硅和水,则将CaMg3Si4O12的氧化物形式为CaO·3MgO·4SiO2。
考点:考查氢氧化亚铁、漂白粉、氨气制备以及硅酸盐表示
考点分析: 考点1:铁及其化合物 考点2:铜及其化合物 考点3:氮族元素 考点4:卤素 考点5:氧族元素 试题属性

科目:高中化学 来源:2014-2015学年广东省中山市高三下学期第二次模拟考试理科综合化学试卷(解析版) 题型:选择题
下表是元素周期表的一部分,有关说法正确的是

A.e的氢化物比d的氢化物稳定
B.a、b、e三种元素的原子半径:e>b>a
C.六种元素中,c元素单质的化学性质最活泼
D.c、e、f的最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长望浏宁四县高三一模考试化学试卷(解析版) 题型:填空题
【化学-选修3物质结构与性质】(15分)早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________方法区别晶体、准晶体和非晶体。
(2)基态Fe原子有_______个未成对电子,Fe3+的电子排布式为_________。可用硫氰化钾检验Fe3+,形成的配合物的颜色为____________。
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道为___________,1mol乙醛分子中含有的 键的数目为___________。乙酸的沸点明显高于乙醛,其主要原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和定点,则该晶胞中有 个铜原子。
键的数目为___________。乙酸的沸点明显高于乙醛,其主要原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和定点,则该晶胞中有 个铜原子。
(4)Al单质为面心立方晶体,其晶胞参数 nm,晶胞中铝原子的配位数为 。列式表示Al单质的密度 g
nm,晶胞中铝原子的配位数为 。列式表示Al单质的密度 g cm-3。
cm-3。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省七市教科研协作体高三3月联考化学试卷(解析版) 题型:实验题
Na2S2O3可用作照相的定影剂等。已知Na2S2O3的某些性质如下:
(Ⅰ)S2O32-能被I2氧化为S4O62-;
(Ⅱ)酸性条件下S2O32-迅速分解为S和SO2;
(Ⅲ)向Na2S2O3和Na2S混合溶液中通入SO2可制得Na2S2O3;所得产品中常含有少量Na2SO3和Na2SO4。
实验室可用如下装置(略去部分夹持仪器)模仿生成过程。
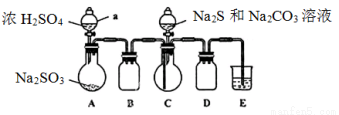
实验步骤:
(1)仪器组装完成后, ,则整个装置气密性良好。装置D的作用是 ,装置E中溶液的作用是 。
(2)先向C中烧瓶加入Na2S2O3和Na2S混合溶液,再向A中烧瓶滴加浓H2SO4。
(3)等Na2S2O3和Na2S完全消耗后,结束反应。过滤C中混合物,将溶液蒸发、结晶、过滤、洗涤、干燥,得到产品。
(4)为验证产品中含有硫酸盐,该小组设计了以下实验方案,请将方案补充完整。
实验步骤 | 预期现象或结论 |
步骤1:取少量固体样品溶于无氧蒸馏水中 | 固体完全溶解得无色澄清溶液 |
步骤2:加入过量盐酸 | |
步骤3:静置后取上清液,加入BaCl2溶液 |
(5)利用KMnO4标准溶液可以定量测定硫代硫酸钠试剂的纯度,步骤为:
①溶液配制:称取1.0g Na2S2O3试样,用新煮沸并冷却的蒸馏水溶解,最终定容至100mL。
②滴定:取10.00mL0.01mol·L-1 KMnO4标准溶液,加硫酸酸化,再加过量KI溶液。写出该反应的离子反应:
③往步骤②所得溶液加入某指示剂,用Na2S2O3滴定至终点(2S2O32- +I2 S4O62- +2I-),记录Na2S2O3溶液用量,滴定3次。指示剂最好选用 ,本次滴定时所用的玻璃仪器除锥形瓶外,还有 。
S4O62- +2I-),记录Na2S2O3溶液用量,滴定3次。指示剂最好选用 ,本次滴定时所用的玻璃仪器除锥形瓶外,还有 。
④若3次滴定Na2S2O3溶液的平均用量为12.00mL,则样品的纯度为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省七市教科研协作体高三3月联考化学试卷(解析版) 题型:选择题
化学来源于生活,也服务于生活,下列有关生活中的化学叙述正确的是
A.冰箱中使用的含氟制冷剂泄露后,会增加空气中的PM2.5
B.浓硫酸具有强腐蚀性,可用浓硫酸刻蚀石英制艺术品
C.施肥时,农家肥草木灰(有效成分K2CO3)不能与氮肥NH4Cl混合使用
D.氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市高三下学期开学联考化学试卷(解析版) 题型:选择题
今有0.1mol/L Na2SO4溶液300mL,0.1mol/L MgSO4溶液200mL和0.1mol/L Al2(SO4)3溶液100mL,这三种溶液中硫酸根离子浓度之比是
A.1:1:1 B.3:2:1 C.3:2:3 D.1:1:3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市高三下学期开学联考化学试卷(解析版) 题型:选择题
在下列反应中,水仅作还原剂的是
A.Na2O+H2O=2NaOH B.2F2+2H2O=4HF+O2
C.Cl2+H2O=HCl+HClO D.2K+2H2O=2KOH+H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:填空题
(8分)恒容体系,发生如下反应2A(g) B(g)+xC(g) ΔH,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图。某课外活动小组一共进行了如图所示的三个实验(其中T1、T2表示不同的反应温度)。
B(g)+xC(g) ΔH,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如图。某课外活动小组一共进行了如图所示的三个实验(其中T1、T2表示不同的反应温度)。

(1)在实验Ⅲ中,0~20min的时间内,v(A)= 。
(2)分析实验I和实验II的数据,可知x= ;分析实验II和实验Ⅲ的数据,可知反应热ΔH 0(选填“>”、“=”或者“<”)。
(3)能说明该反应达到平衡状态的是(选填代号字母) 。
a.A的质量不再变化
b.混合气体的密度保持不变
c.用A、B、C表示的反应速率的比为2∶1∶x
d.单位时间内生成n mol B的同时生成2n mol A
e.混合气体的平均摩尔质量保持不变
(4)T1℃时,保持容器的体积不变,若充入a mol A、b mol B、c mol C,达到平衡时C的体积分数为0.4,则a、b、c应满足什么条件 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com