
向一定量的饱和石灰水中加入少量CaO固体,恢复到原来温度时,下列说法正确的是( )
|
| A. | 溶液中的Ca2+总数不变 | B. | 溶液中 OH﹣数目增加 |
|
| C. | 溶质的物质的量浓度不变 | D. | 溶液的质量不变 |
考点:
溶解度、饱和溶液的概念.
专题:
物质的量浓度和溶解度专题.
分析:
根据题中“向饱和的澄清的石灰水中加入少量氧化钙”后,氧化钙和水反应生成了氢氧化钙,由于反应过程放出大量的热,温度升高;所以恢复到20℃时,原来的饱和溶液中溶剂的质量减少,则原溶液中溶质氢氧化钙固体析出,但现在的溶液仍是饱和溶液,其溶质的质量分数不变.
解答:
解:A、由题意可知:加入氧化钙与溶液中的水反应,致使溶剂减少,有固体氢氧化钙析出,则溶质的质量减少;钙离子数量也会减少,故A错误;
B、根据题意,溶剂减少,致使原饱和溶液中溶质氢氧化钙析出,则溶液中OH﹣数目,故B错误;
C、恢复到20℃时,原来的饱和溶液中溶剂的质量减少,则原溶液中溶质氢氧化钙固体析出,但现在的溶液仍是饱和溶液,所以溶质的物质的量浓度不变;故C正确;
D、氧化钙和水反应生成了氢氧化钙,水减少,则析出氢氧化钙,所以溶液质量减小,故D错误;
故选C.
点评:
本题是考查饱和溶液中加入某物质后,所得溶液中各种成分的变化情况.这里要注意:氧化钙等一些物质与水反应致使溶液中一些成分发生变化,但溶液仍是饱和的,题目难度不大.


科目:高中化学 来源: 题型:
将标准状况下的VL HCl(气)溶于水配成1L溶液,得到的盐酸密度为ρg/cm3,则该盐酸的物质的量浓度为()
A. 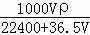 mol/L B.
mol/L B.  mol/L
mol/L
C.  mol/L D.
mol/L D. 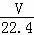 mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
在某2L恒容密团容器中充入2mol X(g)和1mol Y(g)发生反应:2X(g)+Y(g)⇌3Z(g)△H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是()
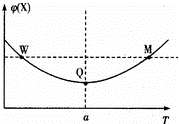
A. 升高温度,平衡常数增大
B. W点Y的正反应速率等于M点Y的正反应速率
C. Q点时,Y的转化率最大
D. 平衡时充入Z.达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制取时,要收集干燥纯净的氯气,应使氯气依次通过( )
|
| A. | 水、浓H2SO4 | B. | 饱和Na2CO3溶液、浓H2SO4 |
|
| C. | 饱和NaCl溶液、浓H2SO4 | D. | 饱和NaHCO3溶液、浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
|
| A. | 甲的分子数比乙的分子数多 |
|
| B. | 甲的物质的量比乙的物质的量少 |
|
| C. | 甲的摩尔体积比乙的摩尔体积小 |
|
| D. | 甲的相对分子质量比乙的相对分子质量小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室配制500mL 0.1mol•L﹣1的Na2CO3溶液,请回答下列问题.
(1)应用托盘天平称取Na2CO3•10H2O晶体 g.
(2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上(1g以下用游码),天平平衡时,则实际称量的Na2CO3•10H2O晶体 g.
(3)用托盘天平和小烧杯称出Na2CO3•10H2O的质量,其正确操作顺序的标号为(操作可以重复) .
A.调整零点 B.将游码移至刻度尺的零刻度处,将砝码放回砝码盒内
C.将碳酸钠晶体放入小烧杯中称量 D.称量空的小烧杯 E.记录称量结果
(4)下列操作对配得的溶液无影响的是 (填序号);会使所配溶液浓度偏大的是 (填序号).
①在烧杯内溶解溶质,搅拌时不慎溅出少量溶液.
②容量瓶未烘干就用来配制溶液.
③定容时俯视刻度线.
④定容时仰视刻度线.
⑤定容时不小心使少量蒸馏水流出瓶外.
⑥将所配溶液从容量瓶转移到干燥、洁净的试剂瓶中时,有少量溅出.
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,该电池长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是()
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是()
A. 放电时负极反应为:Zn﹣2e﹣+2OH﹣=Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3﹣3e﹣+5OH﹣=FeO42﹣+4H2O
C. 放电时每转移1 mol电子,正极有1mol K2FeO4被还原
D. 放电时正极附近溶液的pH值升高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是()
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com