
| A | B | C | D | |
| 电解质溶液 | HCl | AgNO3 | KOH | BaCl2 |
| pH变化 | 减小 | 增大 | 增大 | 不变 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
A、气体物质的量的计算公式:n=
| ||
B、溶液中溶质的物质的量浓度(C)与质量分数(W)换算公式:C=
| ||
| C、KClO3溶于水的电离方程式:KClO3=K++Cl-+3O2- | ||
| D、向澄清石灰水中通入过量CO2反应的离子方程式:Ca2++2OH-+CO2=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按右图装置实验,A、B两烧杯分别盛放200g 10%NaOH和足量CuSO4溶液.通电-段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5g (不考虑水的蒸发).则下列叙述中正确的是( )
按右图装置实验,A、B两烧杯分别盛放200g 10%NaOH和足量CuSO4溶液.通电-段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5g (不考虑水的蒸发).则下列叙述中正确的是( )| A、电源P极为负极 |
| B、标准状况下,b极产生气体的体积为5.6 L |
| C、c极上析出固体的质量为32 g |
| D、a极上所发生的电极反应式为40H--4e-=2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、XY |
| B、XY2 |
| C、XY3 |
| D、XY4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应 |
| B、在同一条件下不同物质有不同的熵值,其体系的混乱度越大,熵值越大 |
| C、一个反应能否自发进行取决于反应吸热还是放热 |
| D、一个反应能否自发进行,与焓变和熵变的共同影响结果有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同浓度,pH由大到小:c>a>b |
| B、同浓度同体积,分别与氢氧化钠中和,所需的氢氧化钠的物质的量由大到小:c>a>b |
| C、同pH,物质的量浓度由大到小:b>a>c |
| D、同pH同体积,分别于少量且质量相同的Zn片反应,反应所需时间由长到短:b>a>c |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
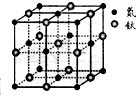 现有5种短周期元素A、B、C、D、E,原子序数依次增大.A的同位素中有一种核素无中子,B最外层上电子数是次外层电子数的两倍,C元素最简单的氢化物Y的水溶液呈碱性,E是短周期中电负性最小的元素.D与可与A、B、C、E四种元素分别形成原子个数比不相同的常见化合物.回答下列问题:
现有5种短周期元素A、B、C、D、E,原子序数依次增大.A的同位素中有一种核素无中子,B最外层上电子数是次外层电子数的两倍,C元素最简单的氢化物Y的水溶液呈碱性,E是短周期中电负性最小的元素.D与可与A、B、C、E四种元素分别形成原子个数比不相同的常见化合物.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com