
据报道,氢燃料电池公交车已经驶上北京街头。下列说法正确的是( )
A.电解水制取H2是理想而经济的制氢方法
B.发展氢燃料电池公交车不需要安全高效的储氢技术
C.氢燃料电池公交车的使用可以减少城市空气污染
D.氢燃料电池把H2和O2燃烧放出的热能转化为电能
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图。
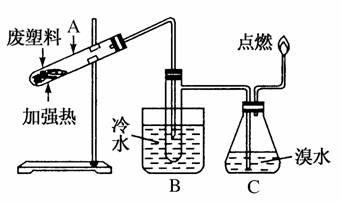
加热聚丙烯废塑料得到的产物如下表所示:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。
A中残留物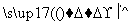



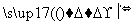 聚乙炔
聚乙炔
写出反应②③的化学方程式:___________________________、____________________________。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,写出其所有一氯代物的结构简式_________________________ _______________________________________。
(3)锥形瓶C中观察到的现象:______________________。经溴水充分吸收,剩余气体经干燥后的平均相对分子质量为________。
(4)写出C中逸出的气体在工业上的两种用途:________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
日本大地震、海啸引发多处核险情。下列说法中正确的是( )
A.核能是一种清洁、环保、安全的新能源
B.核变化属于化学变化
C.氢气的燃烧热最高,且来源丰富、无污染,是一级能源
D.将煤制成气体燃料或液体燃料,可以提高其燃烧效率
查看答案和解析>>
科目:高中化学 来源: 题型:
城市使用的燃料,现大多为煤气、液化石油气。煤气的主要成分是一氧化碳和氢气的混合气,它由煤炭与水(蒸气)反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学反应方程式______________。
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为:
C3H8(g)+5O2(g)===3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1
已知CO气体燃烧的热化学方程式为
CO(g)+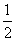 O2(g)===CO2(g)
O2(g)===CO2(g)
ΔH=-282.57 kJ·mol-1
试比较同物质的量的C3H8和CO燃烧,产生的热量比值约为________。
(3)已知氢气燃烧的热化学方程式为
2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6 kJ·mol-1
试比较同质量的氢气和丙烷燃烧,产生的热量比值约为_____。
(4)氢气是未来的能源,除产生的热量多之外,还具有的优点是_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
人类将在未来几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能的转换形态),届时人们将适应“低碳经济”和“低碳生活”。下列说法不正确的是( )
A.煤、石油和天然气都属于碳素燃料
B.发展太阳能经济有助于减缓温室效应
C.太阳能电池可将太阳能直接转化为电能
D.目前研究菠菜蛋白质“发电”不属于太阳能文明
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是一种航天器能量储存系统原理示意图。下列说法正确的是( )
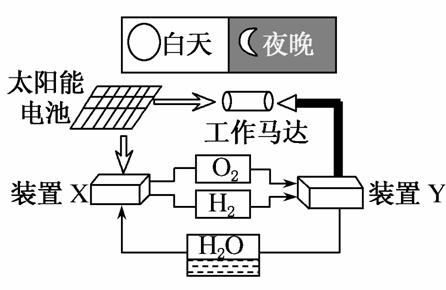
A.该系统中只存在3种形式的能量转化
B.装置Y中负极的电极反应式为:O2+2H2O+4e-===4OH-
C.装置X能实现燃料电池的燃料和氧化剂再生
D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,一定体积的密闭容器中有如下平衡:H2(g)+I2(g)2HI(g)。已知H2和I2的起始浓度均为0.10 mol·L-1,达平衡时HI的浓度为0.16 mol·L-1。则平衡时H2的浓度(mol·L-1)是( )
A.0.16 B.0.08
C.0.04 D.0.02
查看答案和解析>>
科目:高中化学 来源: 题型:
由原子序数由小到大的A、B、C、D、E五种元素构成某配位化合物X,其原子个数比为14:4:5:1:1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-l)dn+61Ns1,回答下列问题。
(1)该配位化合物X的化学式为 。
(2)元素B、C、D的第一电离能的由小到大排列顺序为 。(用元素符号表示)
(3)D元素原子的最外层电子轨道表示式为________ 。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为 。
(5)碳铂是一种含BA3分子的具有抗癌活性的金属配合物,碳铂的结构如下图:其中碳原子的杂化方式有____ 。
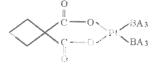 碳铂中含有的作用力有 (填字母)。
碳铂中含有的作用力有 (填字母)。
A.共价键 B.配位键
C.金属键 D.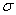 键 E.
键 E.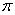 键
键
(6)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1:1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式 。单质E的晶胞如图所示,若设该晶胞的边长为acm,阿伏加德罗常数为NA,单质E的摩尔质量为Mg/mol,则表示该晶胞密度的计算式为p= g/cm3。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com