
”¾ĢāÄæ”æŹµŃéŹŅÓĆÅØĮņĖįŗĶŅŅ“¼ÖĘČ”ŅŅĻ©Ź±£¬³£»į擵½ÉÕĘæÖŠŅŗĢå±äŗŚ£¬ÖʵƵÄŅŅĻ©ÖŠ»ģÓŠCO2”¢SO2µČŌÓÖŹ”£Ä³æĪĶāŠ”×éÉč¼ĘĮĖČēĻĀ×°ÖĆ£¬Ö¤Ć÷ŅŅĻ©ÖŠ»ģÓŠCO2”¢SO2²¢ŃéÖ¤ŅŅĻ©µÄŠŌÖŹ”£
»Ų“šĻĀĮŠĪŹĢā£ŗ
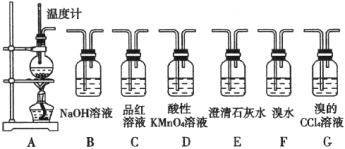
£Ø1£©×°ÖĆAŹĒŅŅĻ©µÄ·¢Éś×°ÖĆ”£Ķ¼ÖŠŅ»“¦Ć÷ĻŌµÄ“ķĪóŹĒ__________£¬ÉÕĘæÖŠĖé“ÉʬµÄ×÷ÓĆŹĒ__________”£
£Ø2£©ČōŅŖ¼ģŃéAÖŠĖłµĆĘųĢåŗ¬ÓŠSO2£¬æɽ«»ģŗĻŗĻĘųĢåÖ±½ÓĶØČė__________(Ģī“śŗÅ£¬ĻĀĶ¬)×°ÖĆ£»ČōŅŖ¼ģŃ飬AÖŠĖłµĆĘųĢåŗ¬ÓŠCH2=CH2£¬æɽ«»ģŗĻĘųĢåĻČĶØČėB×°ÖĆ£¬Č»ŗóĶØČė__________×°ÖĆ”£
£Ø3£©Š”Ć÷½«“ÓA³öĄ“µÄ»ģŗĻĘųĢåŅĄ“ĪĶعżB”¢E”¢D”¢E£¬·¢ĻÖDĒ°ĆęµÄŹÆ»ŅĖ®ÖŠĪŽĆ÷ĻŌ±ä»Æ”¢DŗóĆęµÄŹÆ»ŅĖ®±ä»ė×Ē”£Ēė¶Ō³öĻÖøĆĻÖĻóµÄŌŅņ½ųŠŠŗĻĄķ²ĀĻė__________”£
£Ø4£©Š“³öŹµŃéŹŅÖĘČ”ŅŅĻ©µÄ»Æѧ·½³ĢŹ½__________”£
”¾“š°ø”æ£Ø1£©ĪĀ¶Č¼ĘĖ®ŅųĒņ²æ·Öƻӊ²åČėŅŗĆęŅŌĻĀ£»·Ą±¬·Š
£Ø2£©C D(»ņF»ņG)£Ø3£©ŅŅĻ©±»ĖįŠŌøßĆĢĖį¼ŲČÜŅŗŃõ»Æ³ÉCO2
£Ø4£© CH3CH2OH![]() CH2=CH2”ü+H2O
CH2=CH2ӟ+H2O
”¾½āĪö”æ
ŹŌĢā£Ø1£©ÅØĮņĖįŗĶŅŅ“¼ÖĘČ”ŅŅĻ©Ź±£¬Ó¦ŃĻøńæŲÖĘ·“Ó¦ĪļŅŅ“¼ÅØĮņĖį»ģŗĻŅŗµÄĪĀ¶ČŌŚ170¶Č£¬ĖłŅŌĪĀ¶Č¼Ę²āĮæµÄŹĒ»ģŗĻŅŗµÄĪĀ¶Č£¬ĪĀ¶Č¼ĘĖ®ŅųĒņ²æ·Öƻӊ²åČėŅŗĆęŅŌĻĀ£»ŅŅ“¼·ŠµćµĶ£¬¼ÓČČŹ±ČŻŅ×·¢Éś±¬·Š£¬¼ÓČČĖé“ÉʬæÉŅŌ·ĄÖ¹±¬·Š£¬¹Ź“š°øĪŖ£ŗĪĀ¶Č¼ĘĖ®ŅųĒņ²æ·Öƻӊ²åČėŅŗĆęŅŌĻĀ£»””·ĄÖ¹·¢Éś±¬·Š£»
£Ø2£©ČōAÖŠĖłµĆĘųĢåŗ¬ÓŠSO2£¬ŌņĶص½Ź¢ÓŠĘ·ŗģČÜŅŗµÄCÖŠ£¬æÉŅŌŹ¹Ę·ŗģČÜŅŗĶŹÉ«£»½«»ģŗĻĘųĢåĻČĶØČėB£¬ÓĆĒāŃõ»ÆÄĘĪüŹÕÉś³ÉµÄ¶žŃõ»ÆĮņ£¬Č»ŗóĶØČėŹ¢ÓŠĖįŠŌµÄøßĆĢĖį¼ŲµÄD×°ÖĆ£¬ČōøßĆĢĖį¼ŲĶŹÉ«ŌņæÉÖ¤Ć÷ŅŅĻ©µÄ“ęŌŚ£»¹Ź“š°øĪŖ£ŗC£»D£»
£Ø3£©DĒ°ĆęµÄŹÆ»ŅĖ®ĪŽĆ÷ĻŌ±ä»ÆĖµĆ÷ŅŅ“¼Ģ¼»ÆÉś³ÉµÄ¶žŃõ»ÆĢ¼ŗĶ¶žŃõ»ÆĮņ¶¼±»ĒāŃõ»ÆÄĘĪüŹÕ£¬DŗóĆęµÄŹÆ»ŅĖ®±ä»ģ×Ē£¬ĖµĆ÷»ģŗĻĘųĢåĶØČėµ½ĖįŠŌµÄøßĆĢĖį¼ŲÖŠ·¢Éś·“Ó¦²śÉśĮĖÄܹ»Ź¹³ĪĒåŹÆ»ŅĖ®±ä»ė×ĒµÄĘųĢ壬¶ųŅŅĻ©ŗ¬ÓŠ²»±„ŗĶ¼ü¾ßÓŠ»¹ŌŠŌ£¬Äܱ»øßĆĢĖį¼ŲŃõ»Æ£¬¹Ź“š°øĪŖ£ŗŅŅĻ©±»ĖįŠŌKMnO4ČÜŅŗŃõ»Æ³ÉCO2£»
£Ø4£©ŹµŃéŹŅÖĘČ”ŅŅĻ©µÄ»Æѧ·½³ĢŹ½ĪŖCH3CH2OH![]() CH2=CH2”ü+H2O£¬¹Ź“š°øĪŖ£ŗCH3CH2OH
CH2=CH2”ü+H2O£¬¹Ź“š°øĪŖ£ŗCH3CH2OH![]() CH2=CH2”ü+H2O”£
CH2=CH2ӟ+H2Oӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÖø¶Ø·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A. ±„ŗĶNa2CO3ČÜŅŗÓėCaSO4¹ĢĢå·“Ó¦£ŗCO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
B. Ėį»ÆNaIO3ŗĶNaIµÄ»ģŗĻČÜŅŗ£ŗI +IO3+6H+![]() I2+3H2O
I2+3H2O
C. KClO¼īŠŌČÜŅŗÓėFe(OH)3·“Ó¦£ŗ3ClO+2Fe(OH)3![]() 2FeO42+3Cl+4H++H2O
2FeO42+3Cl+4H++H2O
D. µē½ā±„ŗĶŹ³ŃĪĖ®£ŗ2Cl+2H+![]() Cl2”ü+ H2”ü
Cl2ӟ+ H2ӟ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄĘĄė×Óµē³Ų¾ßÓŠ³É±¾µĶ”¢ÄÜĮæ×Ŗ»»Š§ĀŹøß”¢ŹŁĆü³¤µČÓÅµć”£Ņ»ÖÖÄĘĄė×Óµē³ŲÓĆĢ¼»ł²ÄĮĻ £ØNamCn£©×÷øŗ¼«£¬ĄūÓĆÄĘĄė×ÓŌŚÕżøŗ¼«Ö®¼äĒ¶ĶŃ¹ż³ĢŹµĻÖ³ä·Åµē£¬øĆÄĘĄė×Óµē³ŲµÄ¹¤×÷ŌĄķ ĪŖNa1-mCoO2+NamCn![]() NaCoO2+Cn”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
NaCoO2+Cn”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A.·ÅµēŹ±£¬Na+ĻņÕż¼«ŅʶÆ
B.·ÅµēŹ±£¬øŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖNamCn”Ŗme-=mNa++Cn
C.³äµēŹ±£¬Ņõ¼«ÖŹĮæ¼õŠ”
D.³äµēŹ±£¬Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖNaCoO2-me-=Na1-mCoO2+mNa+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ![]() ĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
ĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. 0.1 mol µÄ![]() ÖŠ£¬ŗ¬ÓŠ
ÖŠ£¬ŗ¬ÓŠ![]() øöÖŠ×Ó
øöÖŠ×Ó
B. pH=1µÄH3PO4ČÜŅŗÖŠ£¬ŗ¬ÓŠ![]() øö
øö![]()
C. 2.24L£Ø±ź×¼×“æö£©±½ŌŚO2ÖŠĶźČ«Č¼ÉÕ£¬µĆµ½![]() øöCO2·Ö×Ó
øöCO2·Ö×Ó
D. ĆܱÕČŻĘ÷ÖŠ1 mol PCl3Óė1 mol Cl2·“Ó¦Öʱø PCl5£Øg£©£¬Ōö¼Ó![]() øöP-Cl¼ü
øöP-Cl¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņŗ¬Fe2+”¢I”¢BrµÄČÜŅŗÖŠĶØČė¹żĮæµÄĀČĘų£¬ČÜŅŗÖŠĖÄÖÖĮ£×ÓµÄĪļÖŹµÄĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ŅŃÖŖba=5£¬Ļ߶Ī¢ō±ķŹ¾Ņ»ÖÖŗ¬ŃõĖį£¬ĒŅ¢ńŗĶ¢ō±ķŹ¾µÄĪļÖŹÖŠŗ¬ÓŠĻąĶ¬µÄŌŖĖŲ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
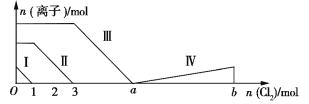
A. Ļ߶Ī¢ņ±ķŹ¾BrµÄ±ä»ÆĒéæö
B. ŌČÜŅŗÖŠn(FeI2)”Ćn(FeBr2)=3”Ć1
C. øł¾ŻĶ¼ĻóĪŽ·Ø¼ĘĖćaµÄÖµ
D. Ļ߶Ī¢ō±ķŹ¾![]() µÄ±ä»ÆĒéæö
µÄ±ä»ÆĒéæö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČĖŌŚ×ö¾ēĮŅŌĖ¶Æŗó£¬ÓŠŅ»¶ĪŹ±¼äĶČŗĶøģ²²»įÓŠĖįÕĶŗĶĢŪĶ“µÄøŠ¾õ”£ŌŅņÖ®Ņ»ŹĒC6H12O6(ĘĻĢŃĢĒ)ŌŚŌĖ¶Æ¹ż³ĢÖŠ×Ŗ»ÆĪŖC3H6O3(ČéĖį)”£4.5gČéĖįÓė×ćĮæµÄÄĘ·“Ó¦£¬ŌŚ±ź×¼×“æöĻĀµĆĘųĢå1120mL”£9gČéĖįÓėĻąĶ¬ÖŹĮæµÄ¼×“¼·“Ó¦£¬Éś³É0.1molČéĖį¼×õ„ŗĶ1.8gĖ®”£ČéĖį±»Ńõ»ÆŹ±µĆ![]() ”£ŌņČéĖįµÄ½į¹¹¼ņŹ½ŹĒ£Ø £©
”£ŌņČéĖįµÄ½į¹¹¼ņŹ½ŹĒ£Ø £©
A. HOCH2CH2COOHB. HOCH2CH(OH)COOH
C. CH3OCH2COOHD. CH3CH(OH)COOH
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČĖĆĒ·¢ĻÖŃõ»ÆĢśĮņøĖ¾śÄÜ“ŁŹ¹»ĘĢśæó(FeS2)Ńõ»Æ³ÉĮņĖįĢśŗĶĮņĖį£¬Ńõ»ÆĢśĮņøĖ¾śÄÜ°ŃæóĪļÖŠµÄĮņ»ņĮņ»ÆĪļŃõ»Æ³ÉĮņĖį£¬¶ųĮņĖįŗĶĮņĖįĢśÄܽ«Ä³Š©æóŹÆÖŠµÄ½šŹōŌŖĖŲ×Ŗ»Æ³É½šŹōĮņĖįŃĪ£¬“Ó¶ųæŖ±ŁĮĖ”°Ļø¾śŅ±½š”±µÄĻČŗÓ”£Ńõ»ÆĢśĮņøĖ¾śµÄ»ī¶Æ¹ż³ĢČēĶ¼ĖłŹ¾£¬ĘäÖŠa¹ż³Ģ·¢ÉśµÄ·“Ó¦ĪŖ4FeS2+15O2+2H2O![]() 2Fe2(SO4)3+2H2SO4”£ŌņĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
2Fe2(SO4)3+2H2SO4”£ŌņĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ

A.a¹ż³ĢÖŠŹĶ·ÅÄÜĮæ
B.Ļø¾śŌŚ·“Ó¦a¹ż³ĢÖŠĘšĮĖ“߻ƼĮµÄ×÷ÓĆ
C.b¹ż³ĢĄąĖĘÓŚÖ²ĪļµÄ¹āŗĻ×÷ÓĆ£¬Ļø¾ś½«ÄÜĮæ“¢“ęŌŚC6H12O6ÖŠ
D.ÓŠŠ©Ļø¾śæÉÖ±½Ó°Ńŗ¬Ē¦”¢¹ÆµČÖŲ½šŹōµÄæóŹÆČܽā£¬µĆµ½ÖŲ½šŹōĄė×ÓµÄČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧѧĻ°Š”×éĄūÓĆČēĶ¼×°ÖĆĄ“ÖʱøĪŽĖ®AlCl3£ØŅŃÖŖ£ŗĪŽĖ®AlCl3178”ęÉż»Ŗ£¬ÓöĖ®ÄÜŃøĖŁ·¢Éś·“Ó¦£©”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
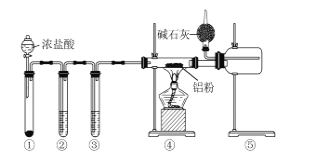
A.×°ÖĆ¢ŁÖŠµÄŹŌ¼ĮæÉÄÜŹĒ¶žŃõ»ÆĆĢ
B.×°ÖĆ¢Ś”¢¢ŪÖŠµÄŹŌ¼Į·Ö±šĪŖÅØĮņĖį”¢±„ŗĶŹ³ŃĪĖ®
C.¢ÜŗĶ¢ŻÖ®¼äŹ¹ÓĆ“Ö²£Į§¹ÜŹĒĪŖĮĖ·Ą¶ĀČū
D.ĒņŠĪøÉŌļ¹ÜÖŠ¼īŹÆ»ŅµÄ×÷ÓĆÖ»ÓŠ“¦ĄķĪ²Ęų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻøß“æ¹čæÉŅŌĶعżĻĀĮŠ·“Ó¦ÖĘČ”£ŗSiCl4£Øg£©+2H2£Øg£©Si£Øs£©+4HCl£Øg£©©236kJ
£Ø1£©·“Ó¦Éę¼°µÄŌŖĖŲŌ×Ó°ė¾¶“ӓ󵽊”µÄÅÅĮŠĖ³ŠņĪŖ_____”£ĘäÖŠ¹čŌ×Ó×īĶā²ćÓŠ_____øöĪ“³É¶Ōµē×Ó£¬ÓŠ_____ÖÖ²»Ķ¬ŌĖ¶ÆדĢ¬µÄµē×Ó£»
£Ø2£©·“Ó¦Éę¼°µÄ»ÆŗĻĪļÖŠ£¬Š“³öŹōÓŚ·Ē¼«ŠŌ·Ö×ӵĽį¹¹Ź½£ŗ_____£»²śĪļÖŠ¾§Ģå¹čµÄČŪµćŌ¶øßHCl£¬ŌŅņŹĒ_____£»
£Ø3£©ĀČŗĶĮņŹĒĶ¬Ņ»ÖÜĘŚŌŖĖŲ£¬Š“³öŅ»øöÄÜ±Č½ĻĀČŗĶĮņ·Ē½šŹōŠŌĒæČõµÄ»Æѧ·½³ĢŹ½£ŗ_____£»
£Ø4£©ŌŚŅ»¶ØĪĀ¶ČĻĀ½ųŠŠÉĻŹö·“Ó¦£¬Čō·“ӦȯĘ÷µÄČŻ»żĪŖ2L£¬3·ÖÖÓŗó“ļµ½Ę½ŗā£¬²āµĆĘųĢåÖŹĮæ¼õŠ”8.4g£¬ŌņŌŚ3·ÖÖÓÄŚH2µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ_____£»
£Ø5£©øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½K£½_____£¬æÉŅŌĶعż_____Ź¹KŌö“ó£»
£Ø6£©Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĆܱÕŗćČŻĘ÷ÖŠ£¬ÄܱķŹ¾ÉĻŹö·“Ó¦Ņ»¶Ø“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ_____”£
a£®vÄę£ØSiCl4£©£½2vÕż£ØH2£©
b£®¹ĢĢåÖŹĮæ±£³Ö²»±ä
c£®»ģŗĻĘųĢåĆܶȱ£³Ö²»±ä
d£®c£ØSiCl4£©£ŗc£ØH2£©£ŗc£ØHCl£©£½1£ŗ2£ŗ4
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com