
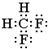 ;下列对于乙的描述正确的是d.
;下列对于乙的描述正确的是d.分析 (1)化合物甲只含C、H两种元素,应为烷烃,分子式符合CnH2n+2,分子中含有26个电子,则有6n+2n+2=26,n=3,则甲为C3H8;
(2)乙分子中C、H、F原子个数比为l:2:2,分子中含有26个电子,应为CH2F2,电子数为26,符合;联系甲烷的空间结构判断CH2F2的结构特点;
(3)将甲、乙按物质的量之比1:1混合所得混合物的平均摩尔质量等于丙的摩尔质量,丙的相对分子质量为:$\frac{44+52}{2}$=48,且分子中含有26个电子,应为C2H5F.
解答 解:(1)化合物甲只含C、H两种元素,应为烷烃,分子式符合CnH2n+2,分子中含有26个电子,则有6n+2n+2=26,n=3,则甲为C3H8,若甲分子中有两个H原子被F原子代替,所得产物可能有CH3CH2CHF2、CH3CF2CH3、CH2FCHFCH3、CH2FCH2CH2F共4种,
故答案为:C3H8;4;
(2)乙分子中C、H、F原子个数比为l:2:2,分子中含有26个电子,其分子式为CH2F2,CH2F2为共价化合物,其电子式为: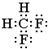 ,
,
为四面体结构,不是正四面体结构,且不存在同分异构体,故a、b、c错误,d正确,
故答案为: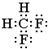 ;d;
;d;
(3)将甲、乙按物质的量之比1:1混合所得混合物的平均摩尔质量等于丙的摩尔质量,丙的相对分子质量为:$\frac{44+52}{2}$=48,且分子中含有26个电子,应为C2H5F,
故答案为:C2H5F.
点评 本题考查有机物分子式、结构简式的确定,题目难度中等,明确烷烃的通式以及原子的构成为解答该题的关键,试题培养了学生的分析、理解能力及灵活应用基础知识的能力.


科目:高中化学 来源: 题型:填空题
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Fe | 稀盐酸 | 偏向Fe |
| 2 | Fe、Cu | CuSO4溶液 | 偏向Cu |
| 3 | Fe、石墨 | 稀盐酸 | ? |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键的类型由元素的类别决定 | |
| B. | 不同种元素组成的多原子分子里的化学键一定是极性键 | |
| C. | 阴、阳离子相互反应形成的化学键称为离子键 | |
| D. | 熔融态下能导电的化合物中一定含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| KSP(25℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| A. | 在pH=5的溶液中.Fe3+不能大量存在 | |
| B. | 混合溶液中c(SO42-):[c(Fe3+)+c(Fe2+)+c(Cu2+)]>5:4 | |
| C. | 向混合溶液中逐滴加入0.1mol•L-1NaOH溶液,最先看到红褐色沉淀 | |
| D. | 向混合溶液中加入适量氯水,并调节pH到3~4过滤,可获较纯净的CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
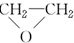 (环氧乙烷).
(环氧乙烷).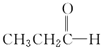 $\stackrel{NaBH_{4}}{→}$CH3CH2CH2OH
$\stackrel{NaBH_{4}}{→}$CH3CH2CH2OH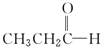 $→_{HCl}^{Zn(Hg)}$CH3CH2CH3
$→_{HCl}^{Zn(Hg)}$CH3CH2CH3查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 混合物 | 试剂 | 分离方法 | |
| A | 溴苯(溴) | 氢氧化钠 | 分液 |
| B | 乙烷(乙烯) | 氢气 | 催化剂、加热 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠 | 分液 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
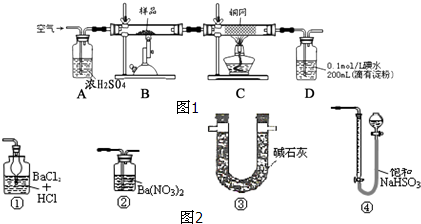
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com