
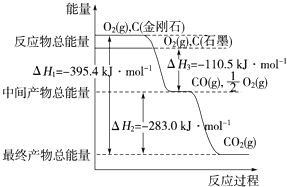
【题目】金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示。下列说法正确的是( )
A.等质量的金刚石和石墨完全燃烧,石墨放出的热量更多
B.在通常状况下,金刚石和石墨相比,金刚石更稳定
C.表示石墨燃烧热的热化学方程式为C(石墨,s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
D.36 g石墨转化成金刚石,放出的热量为5.7 kJ
【答案】C
【解析】
由图可知:1molO2+1molC(金刚石)的能量比1molCO2的能量高395.4KJ,即1molO2和1molC(金刚石)完全反应生成1molCO2放出395.4KJ的能量;1molO2+1molC(石墨)的能量比1molCO+![]() mol O2的能量高110.5KJ,即
mol O2的能量高110.5KJ,即![]() molO2和1molC(石墨)反应生成1molCO放出110.5KJ的能量;1molCO+
molO2和1molC(石墨)反应生成1molCO放出110.5KJ的能量;1molCO+![]() mol O2的能量比1molCO2的能量高283.0KJ,即1molCO和
mol O2的能量比1molCO2的能量高283.0KJ,即1molCO和![]() mol O2完全反应生成1molCO2放出283.0KJ的能量。
mol O2完全反应生成1molCO2放出283.0KJ的能量。
A. 根据图像,金刚石与氧气的总能量大于石墨与氧气的总能量,生成的产物的能量相同,所以金刚石完全燃烧放出的能量多,故A错误;
B. 因为金刚石与氧气的总能量大于石墨与氧气的总能量,而氧气等量,所以金刚石的能量大于石墨的能量,能量越低越稳定,所以石墨稳定,故B错误;
C. 从图可知,![]() molO2和1molC(石墨)反应生成1molCO放出110.5KJ的能量,1molCO和
molO2和1molC(石墨)反应生成1molCO放出110.5KJ的能量,1molCO和![]() mol O2完全反应生成1molCO2放出283.0KJ的能量,则1molO2和1molC(石墨)反应生成1mol CO2放出393.5 KJ的能量。根据燃烧热的定义,表示石墨燃烧热的热化学方程式应写成:C(石墨,s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,故C正确;
mol O2完全反应生成1molCO2放出283.0KJ的能量,则1molO2和1molC(石墨)反应生成1mol CO2放出393.5 KJ的能量。根据燃烧热的定义,表示石墨燃烧热的热化学方程式应写成:C(石墨,s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1,故C正确;
D. 由图可知,金刚石能量比石墨高,所以石墨转化为金刚石应吸收热量, 故D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】探究Al与CuCl2溶液反应,实验如下:下列说法不正确的是( )
实验 | 现象 |
| a.Al片表面附着蓬松的红色固体 b.产生无色气体,起始速率较慢,之后加快 c.反应放热 d.烧杯底部产生少量不溶于稀盐酸的白色沉淀 e.溶液pH降低 |
A.无色气体是H2
B.实验中影响化学反应速率的因素只有两个,分别是浓度和温度
C.白色沉淀的出现与氧化还原反应有关
D.将铝片改为铝粉会加快化学反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物种分布分数![]() (X)=
(X)=![]() 与pH的关系如图所示:
与pH的关系如图所示:

下列说法正确的是
A. 反应HCO3-![]() H++CO32-的lgK=-6.4
H++CO32-的lgK=-6.4
B. pH═8的溶液中:c(Na+)>c(HCO3-)
C. NaHCO3溶液中滴入少量盐酸至溶液显中性:c(Na+)═c(Cl-)
D. 向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要发生的离子反应:HCO3-+OH-═CO32-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某![]() 样品中含有
样品中含有![]() 、
、![]() 和
和![]() 三种杂质的一种或两种,现将
三种杂质的一种或两种,现将![]() 样品加入足量水,样品全部溶解,再加入过量的
样品加入足量水,样品全部溶解,再加入过量的![]() 溶液得到9克沉淀,对样品所含杂质的正确判断是
溶液得到9克沉淀,对样品所含杂质的正确判断是![]()
A.肯定没有![]()
B.肯定没有![]() 和
和![]()
C.肯定没有![]() ,可能有
,可能有![]()
D.肯定没有![]() ,可能有
,可能有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是200mg MnC2O4·2H2O晶体放在坩埚里加热分解时,所得固体产物的质量(m)随温度(t)变化的关系曲线。(已知草酸锰不稳定,但其中锰元素的化合价在300℃以下不变)
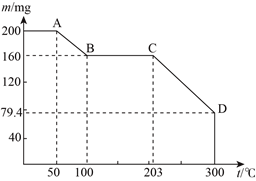
试回答下列问题:
(1)写出B点固体产物的化学式________________________________________;
(2)通过计算确定D点处产物的化学式______________________________。
(3)NaBH4(s)与H2O(l)反应生成NaBO2(s)和H2(g),在25 ℃、101 kPa下,已知每消耗3.8 g NaBH4(s)放热21.6 kJ,该反应的热化学方程式是_____________________________________________。
(4)降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
已知:2NO2(g)![]() N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g)![]() N2O4(l) ΔH2
N2O4(l) ΔH2
下列能量变化示意图中,正确的是(选填字母)________。

(5)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锌是一种重要的工业原料,广泛用于农业、化工、电镀等行业。工业上由锌渣(主要成分为ZnO、FeO、CuO、PbO等)等工业废料生产ZnSO4·7H2O的流程如下:
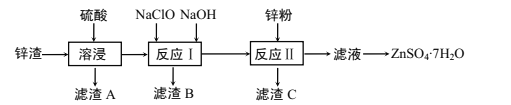
(1)“溶浸”操作中,选用“锌渣”而不选择氧化锌矿粉的原因是______;该操作中不断通入高温水蒸气的目的是________。
(2)“滤渣A”的主要成分是________。
(3)“反应Ⅰ”中,加入NaClO反应的离子方程式为___。
(4)“反应Ⅰ”中,再加入NaOH调节pH约为4.5,则“滤渣B”的主要成分是_____(填化学式)。(Ksp[Zn(OH)2]=3×10-17,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.8×10-39)
(5)“反应Ⅱ”中,加入的锌粉需用少量稀硫酸处理,原因是_________。
(6)取28.7gZnSO4·7H2O加热至不同温度,剩余固体的质量如下表:
温度/℃ | 100 | 250 | 680 | 930 |
质量/g | 17.90 | 16.10 | 13.43 | 8.10 |
则680℃时所得固体的化学式为_________(填字母标号)。
A.ZnO B.Zn3O(SO4)2 C.ZnSO4 D.ZnSO4·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的表达正确的是( )
A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.基态Fe原子的外围电子排布图为![]()
C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大
D.根据原子核外电子排布的特点,Cu在元素周期表中位于s区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气和氨水在工农业生产中均有重要应用。
(1)工业合成氨反应的化学方程式是_________。
(2)实验室常加热熟石灰[主要成分是Ca(OH)2]和氯化铵混合固体制取氨气,写出反应的化学方程式___________。
(3)如图所示,向表面皿中的NaOH固体滴几滴浓氨水,迅速盖上盖,观察现象。

①___________液滴上方会出现白烟(填序号)
A.浓盐酸 B.浓硫酸 C.FeCl3溶液
②一段时间后浓硫酸的液滴中有白色固体,生成该白色固体的化学方程式是_______。
③FeCl3液滴中出现的现象是___________,发生反应的离子方程式是_________。
(4)利用氨水可以将大气污染物SO2吸收并生产氮肥,原理如图所示:
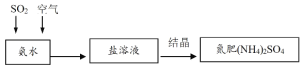
分析上述生产原理,在下列表格中填写该生产过程中利用的SO2的化学性质并进行理论论证
SO2的化学性质 | 理论论证 |
______ | ______ |
______ | ______ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。当其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol![]() 和2mol
和2mol![]() ,开始时容器的体积均为VL,发生如下反应并达到平衡状态
,开始时容器的体积均为VL,发生如下反应并达到平衡状态![]() 提示:物质X,Y的状态均未知,物质Z的状态为气态),2X(?)+Y(?)
提示:物质X,Y的状态均未知,物质Z的状态为气态),2X(?)+Y(?)![]() aZ(g)此时Ⅰ中X,Y,Z的物质的量之比为1:3:2。下列判断正确的是
aZ(g)此时Ⅰ中X,Y,Z的物质的量之比为1:3:2。下列判断正确的是![]()
![]()
Ⅰ Ⅱ
Ⅱ Ⅲ
Ⅲ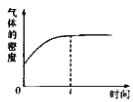
A.物质Z的化学计量数 a= 2
B.若X、Y均为气态,则在平衡时X的转化率:Ⅰ<Ⅱ
C.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y中只有一种为气态
D.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com