
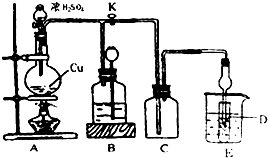
分析 (1)根据铜是金属,具有还原性,浓硫酸具有强氧化性;当C中气体集满,D中逸出二氧化硫;二氧化硫能够与氢氧化钠溶液反应,可以用浸有NaOH溶液的棉团塞在试管口吸收二氧化硫;
(2)B中液体不与二氧化硫反应,也不溶解二氧化硫,据此进行分析;
(3)证明硫酸剩余,需要证明反应后的溶液中存在大量氢离子;
(4)稀硫酸和铜不发生反应,通入氧气后能够反应生成硫酸铜,据此写出反应的化学方程式.
解答 解:(1)铜跟浓硫酸反应,铜具有还原性,浓硫酸具有强氧化性,反应必须加热才能发生,书写化学方程式时注意“浓”字,反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;装置E中试管D内盛品红溶液,当C中气体集满,D中有二氧化硫,二氧化硫能和有色物质品红溶液生成无色物质;二氧化硫有毒,不能直接排放,氢氧化钠溶液能够与二氧化硫反应,可用浸有NaOH溶液的棉团塞在试管口吸收二氧化硫,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;品红溶液褪色;用浸有NaOH溶液的棉团塞在试管口;
(2)装置B的作用是贮存多余的气体,所以B中应放置的液体不能与二氧化硫反应,也不能溶解二氧化硫,而A.饱和Na2SO3溶液、B.酸性KMnO4溶液、C.浓溴水都能够与二氧化硫反应,只有D.饱和NaHSO3溶液符合要求,
故答案为:D;
(3)直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余,证明反应后有硫酸剩余,需要证明反应后的溶液中存在大量氢离子,根据金属活动顺序表可知铁能和氢离子反应,银不与氢离子反应;稀硫酸与BaC12溶液反应生成硫酸钡,但是不能证明是否含有氢离子;与饱和NaHSO3溶液反应生成二氧化硫,证明溶液中含有氢离子,所以AD正确,
故答案为:AD;
(4)实验中甲学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该气体单质具有强氧化性,又是常见的,可以为氧气;铜和氧气、稀硫酸发生氧化还原反应,得到硫酸铜和水,反应的化学方程式为:2Cu+O2+2H2SO4═2CuSO4+2H2O,
故答案为:氧气;2Cu+O2+2H2SO4═2CuSO4+2H2O.
点评 本题考查了浓硫酸的性质,题目难度中等,试题涉及铜与浓硫酸的反应原理、二氧化硫的性质及检验方法、化学方程式的书写等知识,注意掌握浓硫酸具有的性质,明确化学实验基本操作方法.


科目:高中化学 来源: 题型:解答题
 .
. .
.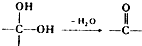 ②
②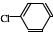 中氯原子较难水解物质A(
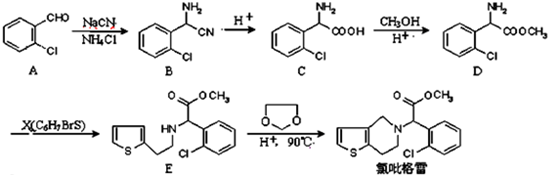
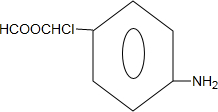
中氯原子较难水解物质A(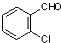 )可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式
)可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式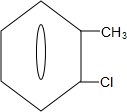 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$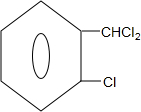 +2HCl;
+2HCl; +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$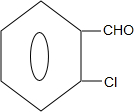 +2NaCl+2H2O
+2NaCl+2H2O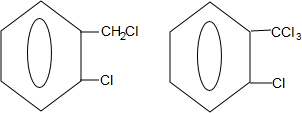
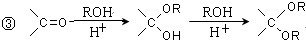
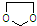 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$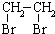
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C5H12的同分异构体数目与甲苯(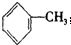 一氯代物的数目相同 一氯代物的数目相同 | |
| B. | CH2═CH2+H20 $\stackrel{一定条件}{→}$CH3CH2OH 属于还原反应 | |
| C. | C3H6Cl2有4种同分异构体(不考虑立体异构) | |
| D. | 石油分馏和煤的干馏均属于物理变化. |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
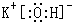 (填写电子式);
(填写电子式);查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18.9 g HNO3 | B. | 3.612×1024个HCl分子 | ||
| C. | 0.2 mol H3PO4 | D. | 0.2 NA个CH4分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 mol | B. | 2.8 mol | C. | 6.4 mol | D. | 3.6 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com