
A.c(Na+)>c(![]() )>c(
)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(
)+c(
C.c(Na+)+c(H+)=c(![]() )+
)+![]() )+c(
)+c(
D.c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
科目:高中化学 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:021
|
下列表示0.1 mol·L-1 NaHSO3溶液中有关微粒浓度的关系式,正确的是 | |
A. |
c(Na+)+c(H+)=c(HSO |
B. |
c(Na+)+c(H+)=c(HSO |
C. |
c(Na+)>c(HSO |
D. |
c(Na+)=c(HSO |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.c(Na+)>c(![]() )>c(
)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(OH-)
)+c(OH-)
C.c(Na+)+c(H+)=c(![]() )+2c(
)+2c(![]() )+c(OH-)
)+c(OH-)
D.c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2CO3)
)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:

(1)NH4Al(SO4)2可作净水剂,其理由是______________________________________________
______________________________(用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH![]() )________0.1 mol·L-1NH4HSO4中c(NH
)________0.1 mol·L-1NH4HSO4中c(NH![]() )。 (填“等于”、“大于”或“小于”)
)。 (填“等于”、“大于”或“小于”)
(3) 用等式表示0.1 mol·L-1NH4Al(SO4)2溶液中各离子浓度关系___________________________
(4)如图是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是________(填写字母),导致pH随温度变化的原因是________________________________________________;
(5)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
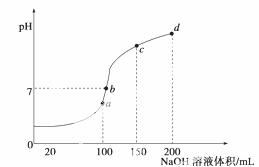
试分析图中a、b、c、d四个点,水的电离程度最大的是____________;在b点,溶液中各离子浓度由大到小的排列顺序是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com