
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)=zC(g)
平衡时测得A的浓度为0.50 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.30 mol/L。下列有关判断正确的是:
A.x+y<z B.平衡向正反应方向移动
C.B的转化率降低 D.C的体积分数下降
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
已知H-H键键能(断裂时吸收或生成时释放的能量)为436 kJ·mol-1,H-N键键能为391 kJ·mol-1,根据热化学方程式:
N2(g) +3H2(g) =2NH3(g) ΔH=-92.4 kJ·mol-1。则N≡N键的键能是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,纯水中的c(H+)=2×10-7 mol/L,下列说法正确的是
A. c(OH-)=2×10-7 mol/L B. c(OH-)=5×10-8 mol/L
C.无法确定OH-浓度 D.该温度低于室温
查看答案和解析>>
科目:高中化学 来源: 题型:
 对于一定条件下的可逆反应2N2O5(g) 4NO2(g) + O2(g) △H>0,在一定条件下达到平衡状态后,若改变条件(未说明的条件不变),对有关物理量及平衡状态有何影响?将变化结果(填增大、减小、不变、变深、变浅),填入空格。
对于一定条件下的可逆反应2N2O5(g) 4NO2(g) + O2(g) △H>0,在一定条件下达到平衡状态后,若改变条件(未说明的条件不变),对有关物理量及平衡状态有何影响?将变化结果(填增大、减小、不变、变深、变浅),填入空格。
(1)压强不变,充入少量氦气,混合气体的颜色 。
(2)升高体系的温度,混合气体的平均相对分子质量 。
(3)使用正催化剂,正反应速率 ,逆反应速率 ,N2O5的转化率 。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲是一种盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。
用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
③取少量甲溶液于试管中加入适量NaOH溶液,加热;
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
回答下列问题:
(1)C的元素符号是 ,D在周期表中的位置 。
(2)用离子方程式表示实验②中现象的原因: 。
(3)实验③中出现的现象是 。
(4)甲中阳离子与阴离子物质的量之比为3:2,则甲的化学式为 。
(5)某同学以氨气和二氧化碳为原料制备碳酸氢铵。合理的方案是
A.先将二氧化碳通入水中,充分溶解后,再通入氨气。
B.先将氨气通入水中,充分溶解后,再通入二氧化碳。
检验产物中有NH4+的方法为
查看答案和解析>>
科目:高中化学 来源: 题型:
设阿伏加德罗常数为NA ,则下列说法正确的是( )
A、常温常压下,11.2 L甲烷中含有的氢原子数为2NA,
B、标准状况下,0.3 mol 二氧化硫中含有氧原子数为0.3NA,
C、4g金属钙变成钙离子时,失去电子数目为0.1NA
D、常温下,1 L 0.1mol·L-1 MgCl2溶液中含有Mg2+ 数为0.1NA,
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上生产MnO2和Zn的主要反应有
① MnO2 + ZnS + 2H2SO4 = MnSO4 + ZnSO4 + S + 2H2O
② MnSO4 + ZnSO4 + 2H2O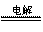 MnO2 + Zn + 2H2SO4
MnO2 + Zn + 2H2SO4
下列说法不正确的是
A.①中MnO2和H2SO4都是氧化剂
B.①中析出16 g S时转移1 mol 电子
C.②中MnSO4发生氧化反应
D.硫酸在该生产中可循环使用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com