
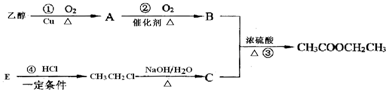
���� �ϳ�����������Ҫ�Ҵ���������Ũ������������ɣ���B��CΪ�Ҵ������B��ˮ��Һ�����ܽ�CaCO3����BΪCH3COOH��CΪCH3CH2OH���Ҵ�����������A����A����������Һ��Ӧ������������AΪ��ȩ��E������ʵ��������ܹ����Ȼ��ⷴӦ���������飬��EΪCH2=CH2���ݴ˽��н��
��� �⣺�ϳ�����������Ҫ�Ҵ���������Ũ������������ɣ���B��CΪ�Ҵ������B��ˮ��Һ�����ܽ�CaCO3����BΪCH3COOH��CΪCH3CH2OH���Ҵ�����������A����A����������Һ��Ӧ������������AΪ��ȩ��E������ʵ��������ܹ����Ȼ��ⷴӦ���������飬��EΪCH2=CH2��
��1��A������Ϊ��ȩ��BΪCH3COOH�����еĹ�����Ϊ�Ȼ�����-COOH������Ӧ��Ϊ�������Ҵ�����������Ӧ���������������÷�ӦҲ����ȡ����Ӧ����Ӧ��Ϊ��ϩ���Ȼ��ⷢ���ӳɷ�Ӧ���������飬
�ʴ�Ϊ����ȩ���Ȼ�����-COOH���� ��������ȡ����Ӧ�����ӳɷ�Ӧ��
��2��A�Ľṹ��ʽΪ��CH3CHO��E�Ľṹ��ʽΪ��CH2=CH2��
�ʴ�Ϊ��CH3CHO�� CH2=CH2��
��3����Ӧ��Ϊ�Ҵ�������������ȩ����Ӧ����ʽΪ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��
��Ӧ��Ϊ��ϩ���Ȼ��ⷢ���ӳɷ�Ӧ���������飬��Ӧ����ʽΪ��CH2=CH2+HCl$\stackrel{һ��������}{��}$CH3CH2Cl��
�ʴ�Ϊ��2CH3CH2OH+O2$��_{��}^{Cu}$2CH3CHO+2H2O��CH2=CH2+HCl$\stackrel{һ��������}{��}$CH3CH2Cl��
���� ���⿼�����л��ƶϣ���Ŀ�Ѷ��еȣ��������ճ����л���ṹ������Ϊ���ؼ���ע����ȷ�����л�����������ơ���Ӧ���ͣ��ܹ���ȷ��д�����л���Ӧ����ʽ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH2=CH-COOH | B�� | CH2=CH-COOCH3 | C�� | CH3CH2OH | D�� | CH2=CH-CH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
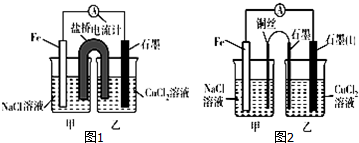
 ���û�ѧ��Ӧԭ���о���Һ����������ʾ�����Ҫ���壮��ش��������⣺
���û�ѧ��Ӧԭ���о���Һ����������ʾ�����Ҫ���壮��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͨ����ˮ���ܷ���ȡ����Ӧ | |
| B�� | ��ϩ˫���е�һ�������Զ��ѣ��������ӳɷ�Ӧ | |
| C�� | ������һ����Ҫ���л��ᣬ��һ����ɫ��ζ��Һ�� | |
| D�� | �����Ҵ����ܶȱ�ˮС�������Ҵ��е�ˮ����ͨ����Һ�ķ�����ȥ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com