
分析 短周期元素A、B、C、D中,0.5mol A元素的离子得到NA个电子被还原为中性原子,则A离子为带2个单位正电荷的阳离子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,由AO+2HCl═ACl2+H2O,可知M(AO)=$\frac{0.4g}{0.01mol}$=40g/mol,所以A的摩尔质量为40g/mol-16g/mol=24g/mol,又A原子核内质子数目与中子数目相等,则质子数为12,即A为Mg元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为Al.Cˉ离子核外电子层数比A元素的离子核外电子层数多1,Cˉ离子核外电子数为18,故C为Cl元素;D元素原子最外层电子数是最内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,则D为C元素,据此解答.
解答 解:短周期元素A、B、C、D中,0.5mol A元素的离子得到NA个电子被还原为中性原子,则A离子为带2个单位正电荷的阳离子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,由AO+2HCl═ACl2+H2O,可知M(AO)=$\frac{0.4g}{0.01mol}$=40g/mol,所以A的摩尔质量为40g/mol-16g/mol=24g/mol,又A原子核内质子数目与中子数目相等,则质子数为12,即A为Mg元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为Al.Cˉ离子核外电子层数比A元素的离子核外电子层数多1,Cˉ离子核外电子数为18,故C为Cl元素;D元素原子最外层电子数是最内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,则D为C元素.
(1)由上述分析可知,A、B、C、D四种元素符号分别为:Mg、Al、Cl、C,
故答案为:Mg;
(2)B的单质是铝单质;C是氯气;D是碳单质,故答案为:Al、Cl、C.
点评 本题考查结构性质位置关系应用,侧重对化学用语的考查,推断元素是解题关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | .①②⑤ | B. | .①③④ | C. | .③④ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、MnO4-、NO3- | B. | Fe3+、A13+、Cl-、HS- | ||
| C. | NH4+、AlO2-、Na+、CH3COO- | D. | K+、Na+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
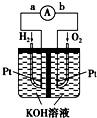 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.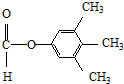 、
、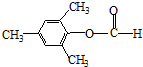 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ④ | C. | ②⑤ | D. | ① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素特征信息 |
| A | 最高正价和最低负价的绝对值之差为2 |
| B | 最外层电子数是内层电子数的3倍 |
| C | 1mol C单质能与冷水反应,在标准状况下生成11.2L H2 |
| D | 原子最外层电子数等于其周期序数 |
| E | 负二价阴离子的电子层结构与Ar原子相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=CHCH3 | B. | CHCl=CHCl | C. | CH3CH=C(CH3)2 | D. | CH3CH2CH=CHBr |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com