
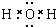 .
.
分析 现有A、B、C、D、E五种短周期元素,它们的核电荷数依次增大,①A是原子半径最小的元素,则A为H元素;②B2是大气中含量最多的气体,B为N元素;它与A可形成10电子的分子,该分子为氨气; ③C与A形成的化合物在常温下为液体,该物质也是10电子的分子,该物质为水,则C为O元素;④D可形成正1价离子D+,D单质与冷水剧烈反应放出氢气,且D的焰色反应呈黄色,则D为Na元素;⑤E和D两种元素可形成离子化合物DE,该化合物的溶液中加入硝酸酸化的A gNO3溶液产生白色沉淀,沉淀是AgCl,则E为Cl元素,据此进行解答.
解答 解:①A是原子半径最小的元素,则A为H元素;②B2是大气中含量最多的气体,B为N元素;它与A可形成10电子的分子,该分子为氨气; ③C与A形成的化合物在常温下为液体,该物质也是10电子的分子,该物质为水,则C为O元素;④D可形成正1价离子D+,D单质与冷水剧烈反应放出氢气,且D的焰色反应呈黄色,则D为Na元素;⑤E和D两种元素可形成离子化合物DE,该化合物的溶液中加入硝酸酸化的A gNO3溶液产生白色沉淀,沉淀是AgCl,则E为Cl元素,
(1)根据分析可知,A为H、B为N、C为O、D为Na、E为Cl元素,
故答案为:H;N; O;Na;Cl;
(2)A与B,A与C形成的10电子分子的物质分别为氨气、水,其化学式分别为:NH3、H2O,
故答案为:NH3;H2O;
(3)A与C形成的10电子分子的化合物为水,水为共价化合物,其电子式为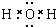 ,
,
故答案为: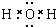 ;
;
(4)DE为NaCl,氯化钠为离子化合物,用电子式表示其形成过程为: ,
,
故答案为:
(5)钠与水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑.
点评 本题考查了位置、结构与性质关系的综合应用,题目难度中等,推断元素为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的分析能力及灵活应用能力.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:选择题
| A. | 向Ba(OH)2溶液滴加NaHSO4溶液至沉淀恰好完全:Ba 2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 用Pt 电极电解MgCl2溶液 2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 往漂白粉溶液中通入少量SO2 Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| D. | 苯酚钠溶液与氯化铝溶液反应 3C6H5O-+Al3++3H2O═3C6H5OH+Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L SO3中含有的分子数为NA个 | |
| B. | 标准状况下,2.24 L NH3和CH4的混合气体,所含电子总数为2NA | |
| C. | 7.1 g Cl2与足量的铁反应转移的电子数目是0.3NA | |
| D. | 1 mol C5H12分子中共价键总数为16NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
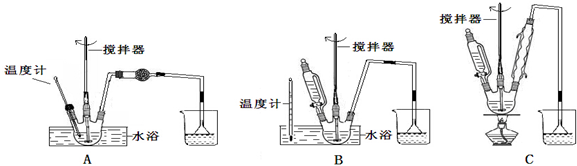
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水、易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
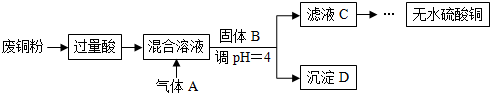
| A. | “过量酸”不适合用硝酸或浓硫酸,固体B可以用CuO、Cu(OH)2或Cu2(OH)2CO3 | |
| B. | 通入的气体A可以是O2或Cl2 | |
| C. | 通入气体A之前的混合溶液中存在的阳离子是:Fe2+、Cu2+、H+ | |
| D. | 将从溶液中得到的硫酸铜晶体在空气中加热,可制得无水硫酸铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硝酸盐是还原剂 | B. | 维生素C是氧化剂 | ||
| C. | 维生素C被氧化 | D. | 亚硝酸盐发生氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com