
| A. | 易失去电子的物质 | B. | 原子核外有10个电子的微粒 | ||
| C. | 原子的最外层只有1个电子的元素 | D. | 原子核内有13个质子的元素 |
分析 A.易失电子的物质不一定是金属元素;
B.原子核外有10个电子的微粒不一定是金属元素;
C.原子的最外层只有一个电子的元素不一定是金属元素;
D.原子核内有13个质子的元素是Al.
解答 解:A.易失电子的物质不一定是金属,如氢气,故A错误;
B.原子核外有10个电子的微粒不一定是金属,如HF等,故B错误;
C.原子的最外层只有一个电子的元素不一定是金属元素,如H,故C错误;
D.原子核内有13个质子的元素是Al,为金属元素,故D正确;
故选D.
点评 本题考查原子、元素、元素周期表等知识点,明确原子、元素周期律结构是解本题关键,采用举例法分析解答,注意规律中的反常现象,易错选项是C.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 ,CCH3CH3,D
,CCH3CH3,D .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2OH | B. | (CH3)3CCH2OH | C. | HOCH2CHBrCH3 | D. | CH3OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉的有效成分是氯酸钙 | |
| B. | 将过量铁粉加入稀硝酸中,有气体生成,充分反应后滴加KSCN溶液,溶液呈血红色 | |
| C. | 将铜粉加1.0mol•L-1Fe2(SO4)3溶液中,溶液变蓝、有黑色固体出现 | |
| D. | 二氧化硅是制造光导纤维的材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
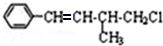
| A. | 1mol 该有机物在加热和催化剂作用下,最多能和3.5molH2反应 | |
| B. | 该有机物分子式为C11H15Cl | |
| C. | 该有机物遇硝酸银溶液产生白色沉淀 | |
| D. | 该有机物能通过消去、加成、水解三步反应生成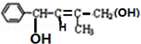 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 存在0.5 mol的CO | B. | 存在0.25 mol的Na2CO3 | ||
| C. | 存在0.125 mol的O2 | D. | 存在0.75 mol的Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰与二氧化硅晶体熔化时,所克服的微粒间相互作用不相同 | |
| B. | 白磷(P4)分子是正四面体结构,故分子中的键角为1090281 | |
| C. | CsCl晶体中每个Cs+周围紧邻的Cl-和每个Cl-周围紧邻的Cs+个数相等 | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:S2->Na+ | B. | 热稳定性:HCl>HF | ||
| C. | 酸性:H3BO3>H2CO3 | D. | 碱性:Al(OH)3>Ca(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com