
 ��
�� ��S2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-��
��S2-+H2O?HS-+OH-��HS-+H2O?H2S+OH-�� 2Na+Cl2����NaH����ˮ���ҷ�Ӧ����NaOH��H2�����������������뻹ԭ�����ռһ�룬����33.6L����״���£���������ʱ����Ӧ��ת�Ƶĵ�����Ϊ
2Na+Cl2����NaH����ˮ���ҷ�Ӧ����NaOH��H2�����������������뻹ԭ�����ռһ�룬����33.6L����״���£���������ʱ����Ӧ��ת�Ƶĵ�����Ϊ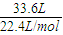 ×
× ×2×NAmol-1=1.5NA��
×2×NAmol-1=1.5NA�� 2Na+Cl2����1.5NA��
2Na+Cl2����1.5NA��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪X��Y��Z��W�Ƕ����������ַǽ���Ԫ�أ����ǵ�ԭ��������������XԪ��ԭ�Ӽ۵����Ų�ʽΪns1��YԪ���ǿ����к�������Ԫ�أ�Z ��Wͬ���壬����Wԭ�ӵĵ����Ų�ʽ�У�p�����ֻ��1��δ�ɶԵ��ӣ�
��֪X��Y��Z��W�Ƕ����������ַǽ���Ԫ�أ����ǵ�ԭ��������������XԪ��ԭ�Ӽ۵����Ų�ʽΪns1��YԪ���ǿ����к�������Ԫ�أ�Z ��Wͬ���壬����Wԭ�ӵĵ����Ų�ʽ�У�p�����ֻ��1��δ�ɶԵ��ӣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�




�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�ر�� | �����Ϣ |
| X | X��һ�ֺ���������Ϊ14��������Ϊ7 |
| Y | Y�Ĺ���������һ�ֵ���ɫ���壬������������ |
| Z | Z�Ļ�̬ԭ��M���������L����2�� |
| W | W�Ļ�̬ԭ�ӵļ۵����Ų�ʽΪ3d104sl |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com