
(5分)将一块金属钠投入到100ml MgCl2和AlCl3的混合溶液中,发现沉淀先多后少。反应完毕后收集到13.44L气体(标准状态),同时得到21.4g白色沉淀,将此沉淀溶于过量的NaOH溶液中,充分反应后沉淀质量减轻了15.6g。求原溶液中Mg2+、Al3+、Cl-的物质的量浓度。
1mol/L 3mol/L 11mol/L
【解析】
试题分析:Na投入到溶液中,首先发生反应:2Na+2H2O=2NaOH+H2↑;n(H2)= 13.44L÷22.4L/mol=0.6mol,n(NaOH)=1.2mol。n(Mg(OH)2)=( 21.4g -15.6g )÷58g/mol=0.1mol;c(Mg2+)=0.1mol ÷0.1L=1mol/L ;使Mg2+形成沉淀消耗的NaOH的物质的量是0.2mol;后来被加入的NaOH溶解的氢氧化铝的物质的量为n(Al(OH)3)= 15.6g÷78g/mol=0.2mol。其中消耗的NaOH是0.2mol×3=0.6mol; 则使Al3+先形成沉淀,后又溶解消耗的NaOH的物质的量为1.2mol-0.2mol-0.6mol=0.4mol。根据方程式:Al3++4OH-=AlO2-+ 2H2O可知溶解消耗的Al3+的物质的量为0.1mol,所以原溶液中含有的Al3+的物质的量为0.2mol +0.1mol= 0.3mol。c(Al3+)=0.3mol÷0.1L=3mol/L;含有的Cl-的物质的量为:n(Cl-)=2n(MgCl2)+ 3n(AlCl3) = 0.1mol×2+0.3mol×3=1.1mol,所以c(Cl-)=1.1mol÷0.1L=11mol/L.
考点:考查金属Na与水的反应及产物与MgCl2和AlCl3反应的情况、物质的量的有关计算的知识。


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源:2013-2014黑龙江省双鸭山市高二下学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.0.01mol/L NH4Al(SO4)2溶液与0.02 mol/LBa(OH)2溶液等体积混合产生沉淀:
NH4++Al3++2SO42?+2Ba2++4OH?=2BaSO4↓+ Al(OH)3↓+NH3·H2O
B.NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O
C.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀: 2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
D.向FeCl3溶液中加入Na2S溶液产生沉淀:2Fe3++3S2-+6H2O=2Fe(OH)3↓+3H2S↑
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省双鸭山市高一下学期期末考试化学试卷(解析版) 题型:选择题
在“绿色化学”工艺中,理想的状态是反应物中的原子全部转化为期望的最终产物,即原子的利用率为100%。下列反应类型中能体现“原子经济性”原则的是( )
①置换反应 ②化合反应 ③分解反应 ④取代反应 ⑤加成反应 ⑥加聚反应
A.①②⑤ B.②⑤⑥ C.③④ D.只有⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西西安铁一中、铁一中国际合作校高三四月月考化学试卷(解析版) 题型:填空题
(15分)X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,已知:
①X元素与Q处于同一主族,其原子价电子排布式都为ns2np2,且X原子半径小于Q的。
②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有1个未成对电子。
③Z元素的电离能数据见下表(kJ·mol-1):
I1 | I2 | I3 | I4 | … |
496 | 4562 | 6912 | 9540 | … |
请回答:
(1)XY2分子空间构型为 ,X原子的轨道杂化方式为 ;QX的晶体结构与金刚石的相似,其中X原子的杂化方式为 ,微粒间存在的作用力是 。
(2)晶体ZW的熔点比晶体XW4明显高的原因是 。
(3)氧化物MO的电子总数与QX的相等,则M为______________(填元素符号)。MO是优良的耐高温材料,其晶体结构与ZW晶体相似。MO的熔点比CaO的高,其原因是_________________________。
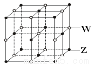
(4)ZW晶体的结构示意图如右图。已知:ρ(ZW)=2.2 g·cm-3,NA=6.02×1023mol-1,则ZW晶体中两个最近的Z离子中心间的距离为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西西安铁一中、铁一中国际合作校高三四月月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.加入Mg能放出H2的溶液:Na+、Al3+、Cl-、SO42-
B.常温下,c(H+)/c(OH-)=1010的溶液:Fe2+、K+、NO3-、SO42-
C.加入苯酚显紫色的溶液:NH4+、K+、Cl-、S2-
D.使甲基橙呈红色的溶液:NH4+、Na+、AlO2-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西西安铁一中、铁一中国际合作校高三五月月考化学试卷(解析版) 题型:选择题
分子式为C4H8O3的有机物,一定条件下具有如下性质:①在浓硫酸存在下,能分别与CH3CH2OH或CH3COOH反应;②在浓硫酸存在下,能脱水生成一种能使溴水褪色的物质,该物质只存在一种结构形式;③在浓硫酸存在下,能生成一种分子式为C4H6O2的五元环状化合物。则C4H8O3的结构简式为
A.HOCH3COOCH2CH3 B.CH3CH(OH)CH2COOH
C.HOCH2CH2CH2COOH D.CH3CH2CH(OH)COOH
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西西安铁一中、铁一中国际合作校高三五月月考化学试卷(解析版) 题型:选择题
一定条件下,可逆反应X(g) + 3Y(g)  2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
A.c1:c2 = 1:3 B.平衡时,Y和Z的生成速率之比为3:2
C.X、Y的转化率不相等 D.c1的取值范围为0 < c1 < 0.14mol/L
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省高一第二学期期末化学试卷(解析版) 题型:填空题
(13分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式: _______________________________
(2)若将(1)中的反应设计成原电池,请在方框内画出原电池的装置图,标出正、负极及材料、电解质溶液并写出电极反应式。

正极反应____________________________;
负极反应____________________________。
(3)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答下列问题:
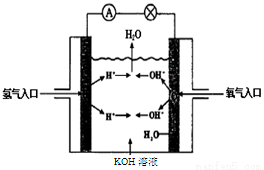
①负极反应式为  溶液PH (填“增大”、“不变”或“减小”)。
溶液PH (填“增大”、“不变”或“减小”)。
②该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2  2LiH Ⅱ.LiH+H2O=LiOH+H2↑
2LiH Ⅱ.LiH+H2O=LiOH+H2↑
反应Ⅰ中的还原剂是 ,7 gLi可吸收标况下H2 L,此时转移电子 moL。
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省延安市第一学期期末考试高二化学试卷(解析版) 题型:选择题
下列说法正确的是

A.上图所示的是一个放热反应 B.加入催化剂v(正)增大、v(逆)减小
C.燃烧热是生成1molH2O放出的热量 D.只有活化分子才能发生有效碰撞
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com